(原标题:新药获批为阿尔茨海默治疗带来重大变革,早期检测首当其冲?| 见智研究所)
1994年11月5日,时已离任5年的美国前总统里根趁自己仍能书写,落笔撰下给公众的最后一封信。信里满是作为病人艰难的剖白。“……我将走向人生的日落。不幸的是,随着阿尔茨海默症的日益严重,我的家庭将不得不承受难以想象的负担。我只是希望能有一些办法将南希从这种痛苦中解脱出来……”
在此之后,里根病情更是快速加深。直至2004年6月5日去世,这位政治名人在生命最后的岁月里,不能自行穿衣、进食、丧失记忆,甚至完全丧失了说话能力。对其亲人而言,这场漫长的告别里充满了不断反复的伤痛,比暗杀更加残忍。
——摘自《南希·里根-漫长的告别》
1906年11月3日,德国医生爱罗斯·阿尔茨海默进行了医学史上首次关于阿尔茨海默症的病理学和临床症状演说。这场演说的大部分内容基于1901~1906年间,阿尔茨海默对一位短期失忆症患者的追踪诊断。患者没有时间和地点的认知能力,也几乎不能记住与自己有关的生活细节。研究的重大转折发生在1906年4月病患去世后。在其家属授权下,阿尔茨海默对遗体脑部进行分析,观察到淀粉样斑块病变和神经原纤维缠结。
医学界自此展开了对阿尔茨海默症持续一百一十多年的研究。阿尔茨海默症被发现是一种发病进程缓慢、随著时间不断恶化的神经退化性疾病。最常见的早期症状为丧失短期记忆,当疾病逐渐进展,其它症状逐渐出现,包括语言障碍、定向障碍、情绪不稳、丧失动机、无法自理和许多行为问题。
截至2020年,全球有约4000万人患有阿尔茨海默症。阿尔茨海默发病年龄多在65岁以上,中度以上病患因严重失去自理能力,生活只能依赖密切看护;每年因此死亡的老年病患达百万人。在发达国家,阿尔茨海默症已成为消耗最多社会资源的疾病之一。
阿尔茨海默病(AD)的病征与病程目前已十分清晰,然而其根源病因和致病机理方面仍有太多问题未达成定论。一直以来,临床医学缺乏实现病程逆转的通用治疗方案,只有少数药物可以对部分病人起到改善效果,
从21世纪伊始,大型医药公司对阿尔茨海默症发起了雄心勃勃的多项药物研发,然而产出却纷纷折戟。近在眼前的,比如2012年强生和辉瑞的针对阿尔茨海默症单抗药物于III期临床一败涂地;2014年,瑞士制药巨头罗氏的单抗药物在大型III期也以失败告终;2016年底,礼来广受瞩目的阿尔茨海默病新药在III期临床试验中功亏一篑。在2003年至2020年间,没有一款药物能通过临床程序获得美国FDA批准上市。
直到2021年6月7日,Biogen(渤健)的单抗药物Aducanumab得到FDA批准,获得适用于治疗早期阿尔茨海默症的生物制品许可(BLA),成为十七年来首个获得FDA批准的治疗阿尔茨海默症海默症新药。
阿尔茨海默病的治疗难点在于其发病机制并非完全清晰。目前,比较公认的理论主张,大脑中的β淀粉样蛋白(amyloid-β,Aβ)生成和清除失衡是神经元变性与痴呆发生的始动因素。Aducanumab是一种高亲和力、靶向- Aβ构象表位的全人IgG1单克隆抗体。它理论上能够有选择性地与AD患者大脑中的淀粉样蛋白沉积结合,然后通过激活免疫系统,一定程度清除大脑中的沉积蛋白。
起先Biogen已经宣布Aducanumab单抗的临床研究失败,但公司医学数据统计师在分析了更大的数据集之后,发现在EMERGE研究中,接受高剂量Aducanumab治疗的阿尔茨海默症患者在第78周的临床知能障碍评定得分(CDR-SB)与对照组相比显著降低了23%,到达了主要终点。另外在其他几项次要终点指标上,高剂量Aducanumab治疗组较安慰剂也显示出了持续降低的效应。
与此同时,影像数据也显示,Aducanumab治疗组第26周和78周的淀粉样蛋白斑负担水平较安慰剂组有明显减轻。虽然充满争议,FDA综合上述数据,最终决定批准了Aducanumab上市。
Aducanumab的出现增加了临床延缓阿尔茨海默症病程发展的手段,但暂时没有证据表明这一药物具备逆转病灶和缓解病征的潜力。在无法逆转病灶这一前提下,延缓病程仅能解决阿尔茨海默症带来问题的一部分,及早治疗就变得尤为关键。在目前,检测技术上的瓶颈严重制约着对阿尔茨海默症的预防和治疗。
缺乏有效的早期临床诊断,大部分患者会错过治疗的最佳有效期,进入不可逆转的轻度乃至中度认知障碍,之后开始接受诊治。因此,阿尔茨海默的早期诊断将成为未来治疗的极关键一步,重要性类比癌症早筛。
阿尔茨海默症的病程分为症状前阶段 (pre-symptomatic phase)、前驱阶段 [prodromal phase,又称轻度认知障碍(MCI, mild cognitive impairment)]以及痴呆阶段(dementia),整个病程可长达20~30年。
美国国家老龄化研究所-痴呆症协会(NIA-AA)在2011年发布的指南,以及中国痴呆与认知障碍指南写作组于2018年发布的文献,都将临床表型与体内阿尔茨海默病病理改变结合,共同构成阿尔茨海默症的诊断标准。体内阿尔茨海默病病理改变可选择的检测方法有脑脊液标志物检测,淀粉样蛋白PET-CT成像等。
具体来看,国际通用的NIA-AA标准将这些生物标志物分为两类:
(1) 脑Aβ沉积的标志物:脑脊液Aβ42,反映皮层β-淀粉样蛋白(amyloid β-protein,Aβ)沉积;Aβ-PET ,提供淀粉样斑块在大脑的分布和含量。
(2) 神经元损伤的生物标志物:脑脊液tau蛋白,反映神经变性的密度;FDG(氟脱氧葡萄糖)-PET,测量神经元和胶质细胞的葡萄糖消耗;Tau-PET,显示特定tau蛋白的扩散状况,Tau-PET目前主要用于临床药物试验。
脑脊液标志物可直接从脑脊液样本中检测,三种PET(正电子发射断层扫描)则采用PET-CT技术,对大脑引入带放射性核素的示踪药物进行显像,然后使用CT解剖结构进行联合诊断。然而两种方式的实施对患者均算不上特别友好——脑脊液标志物检测的样本需要通过脊腰椎穿刺提取;PET-CT价格高昂,单次动辄上万元。过大的感官代价和难以承受的费用,严重阻碍了推广和采用。
不仅如此,对于处于阿尔茨海默症状前阶段或轻度认知障碍阶段的患者,仅能在其脑脊液 (cerebrospinal fluid, CSF) 或血液中检测到β-淀粉样蛋白 (amyloid-β, Aβ)、微管相关蛋白 (tau protein, Tau) 等因子变化,影像学在此阶段作用十分有限。加上处于该阶段的病人认知功能没有或仅轻微受损,现实中将诊断提前的有效早期检测更是稀少。
因此,对于早期诊断,可准确反映病程、且更加易于执行的标志物检测手段,或可打破现阶段两种主要检测方式各自的适用困境。根据相关文献,外周血抗体和外泌体检测已成为当前阿尔茨海默症检测的前沿方向。
与脑脊液检测相比,外周血及外泌体检测所用标志物大体相似,如Aβ含量、Tau蛋白等,标志物在采样样本中含量还相对较低。但两种新检测手段好处在大幅降低于身体侵入,病人在检测全程中基本无痛苦。此外,肿瘤坏死因子(TNF-α)、载脂蛋白E(APOE)、血小板APP比值、可溶性低密度脂蛋白受体相关蛋白(SLRP)等新的标志物,一定程度上也提高外周血等检测阿尔茨海默症的灵敏度带来了可能性。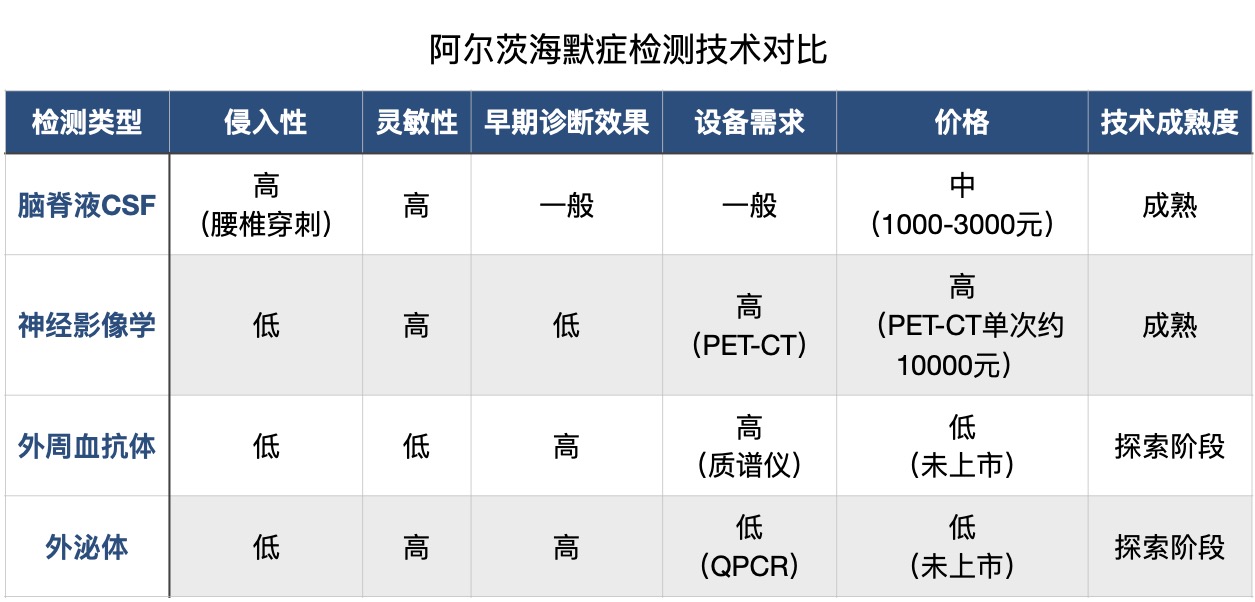
对于新的检测技术,Biogen已有相当关注,公司内部人士曾表示未来不排除会推进外周血检测作为启动药物治疗的判断手段,虽然目前还未确认合作伙伴与最终方案。
根据相关资料,2019年1月29日,C2N Diagnostics公司的血液Aβ42/Aβ40质谱检测获得了FDA突破性设备资格。C2N公司通过用质谱方法检测血液中Aβ42/Aβ40浓度比例,从而对敏感人群进行初筛,有效降低昂贵的淀粉样蛋白PET成像的使用,降低医疗支出。如果后续成果得到FDA批准,将是第一个获批应用于阿尔茨海默病诊断的血液检测方法。
中国的质谱检测公司豪思生物在今年6月10日完成2亿B+轮融资,公司已自主研发了阿尔茨海默症早期独家检测产品。据称这款产品能够在临床症状出现前检出AD并准确分期,根据分期及时制定个体化治疗方案,并通过实时监测,对方案进行精确调整。
除了前沿检测方法外,传统诊断方式也将在国内开始普及。近期,浙江省医保局披露通知决定将PET-CT纳入大病保险支付范围,价格调整为5300元/次,并于7月1日起执行。PET-CT加入医保,有望大幅提升阿尔茨海默症患者检测的可及性。
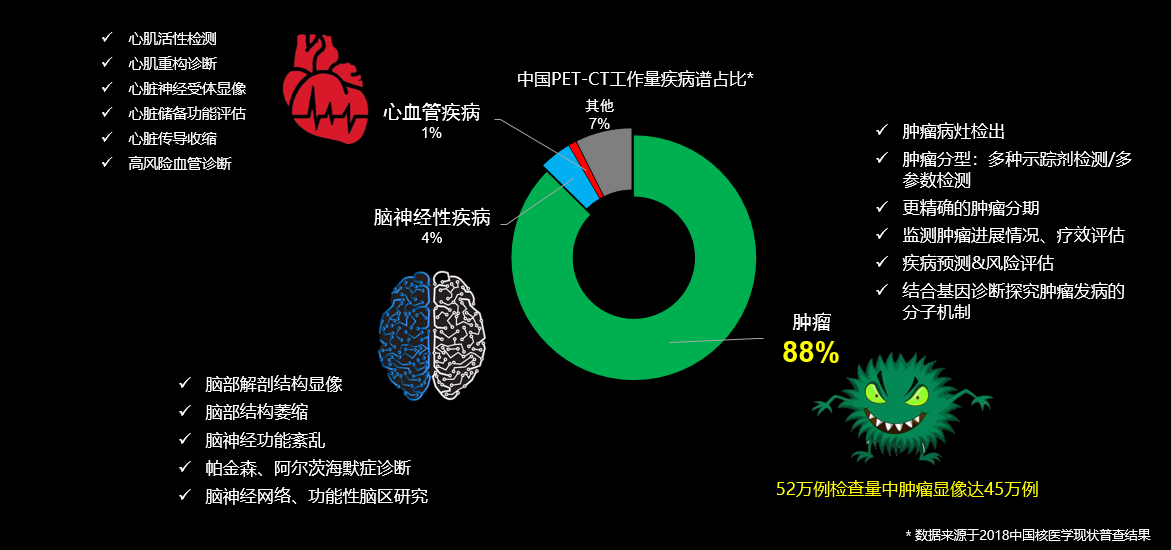
神经系统疾病诊断是PET-CT第二大临床用场景。在Biogen的Aducanumab和礼来的Donanemab临床亚组分析中,均包括β-淀粉样蛋白与Tau PET检测,作为临床患者入组以及药效观测的重要依据。Aducanumab获批及后续在研产品,有望带动相关示踪药物在临床诊断的应用。

目前,应用于β-淀粉样蛋白诊断的示踪药物,全球范围内已有3款获批上市,分别是礼来的florbetapir F18,GE的flutemetamol F18,以及拜耳的florbetaben F18。三款药物未在国内提交临床注册。
据相关行业信息,东诚药业参股(16%)的APRINOIA Therapeutics正在开发针对Tau蛋白PET示踪剂(18F-APN-1607),目前已被FDA认定为“孤儿药”,在美国与台湾同步进行二期临床试验。2020年10月该产品在中国获得三期临床批件(国内唯一临床注册产品),预计明年有望于国内完成入组,继而填补国内相关空白。后续中国CMO业务也将由东诚药业完成。
曙光已来,随着阿尔茨海默症检测方法的进步,低成本和易用性或将使AD早筛进入人们的视野,相信通过及早干预,延缓甚至阻断阿尔茨海默症恶化都将在未来成为可能。
参考资料:
生命科学:阿尔茨海默病生物标志物研究进展(浙江大学脑科学与脑医学学院)
中国阿尔茨海默病痴呆诊疗指南(2020年版)
头豹研究院:中国阿尔茨海默症诊断行业概览
平安证券:东诚药业参股优质核药研发平台,核药版图再补强
《南希·里根:漫长的告别》——帕蒂·戴维斯
