(原标题:不同PD-1单抗在PDB样本医院的销售变化)
前些天跟踪行业时发现PDB更新2022全年数据了,就顺带着梳理一遍上市公司获批新药在样本医院的销售情况。那些这2年才获批的未通过国谈进医保的新药,可能连药事会都还没过而且还有控药占比的压力,只能在院边店或DTP药房卖,PDB数据参考意义很差;但对那些已经上市多年且已经通过国谈进医保的创新药,PDB数据能提供很多有价值的变化信号。下面以国产PD1为例,看下不同PD1单抗在PDB样本医院的销售变化。
下图是12款国内已上市PD1/PDL1单抗在PDB样本医院的年度销售数据变化,几款主流的国产PD1在2021年国谈中大降价,导致2022年样本医院PD1/PDL1总规模增速明显放缓。
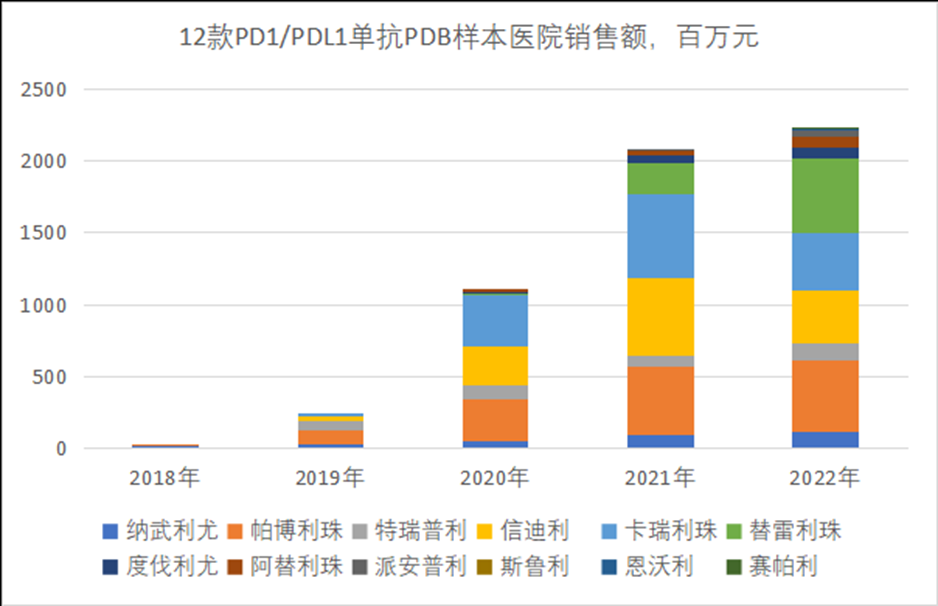
不过,2022年国谈中PD1价格整体不再大降(或已探出行业性的定价底),再加上2021年后获批的派安普利、斯鲁利、恩沃利等住进入院和进医保,预计2023-2024年样本医院PD1/PDL1总市场会恢复强增长。
和2021年相比,不进医保不降价的纳武利尤(O药)、帕博利珠(K药)份额保持稳定,特瑞普利小幅反弹,卡瑞利珠和信迪利份额明显下降,只有替雷利珠份额大增。
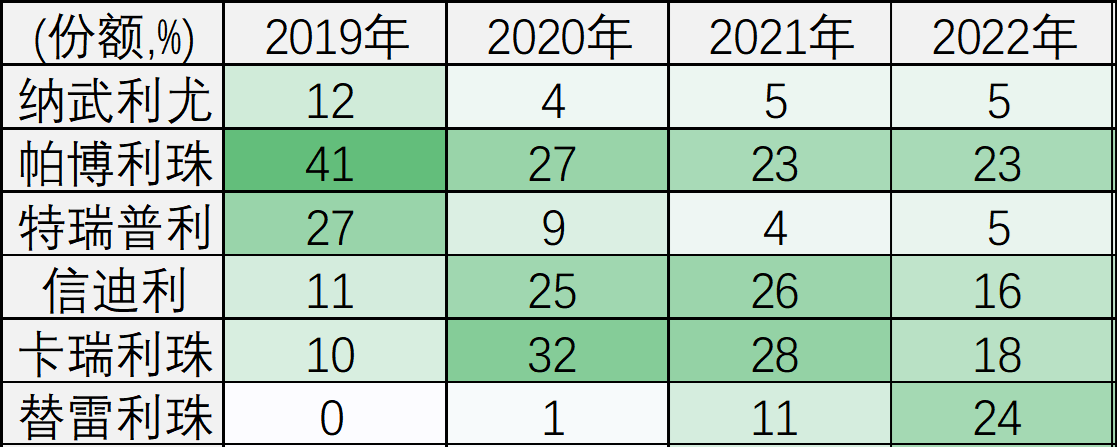
替雷利珠在首批4家国产PD1单抗中获批最晚,但过去3年PDB份额上升最猛,2021年的份额飙升主要是院外回院内驱动,并非终端增长这么多倍;但2022年的份额却是主要来自于实打实的终端销量大增,份额上已经反超帕博利珠、卡瑞利珠、信迪利,成为样本医院中份额第一的PD1单抗。替雷利珠为何能够强势反超?这个现象很值得思考。
一种典型的解释,是销售力的差异。但客观地说,信迪利和卡瑞利珠所属公司的终端销售能力完全不逊替雷利珠。而且如果简单解释成销售能力差异,也无法解释替雷利珠同公司的另一款产品泽布替尼 -- 2022年国内营收增速远低于奥布替尼(+56% VS +164%),这里相差100个点的增速差异,不是一句体量不同就能解释的。
另一种,从产品力的角度去解释,可能更为合理。终端医生并不认同所有PD1单抗能够等同替换,对他们来说,Fc改造更合理的替雷利珠的整体性能或许更值得信赖。
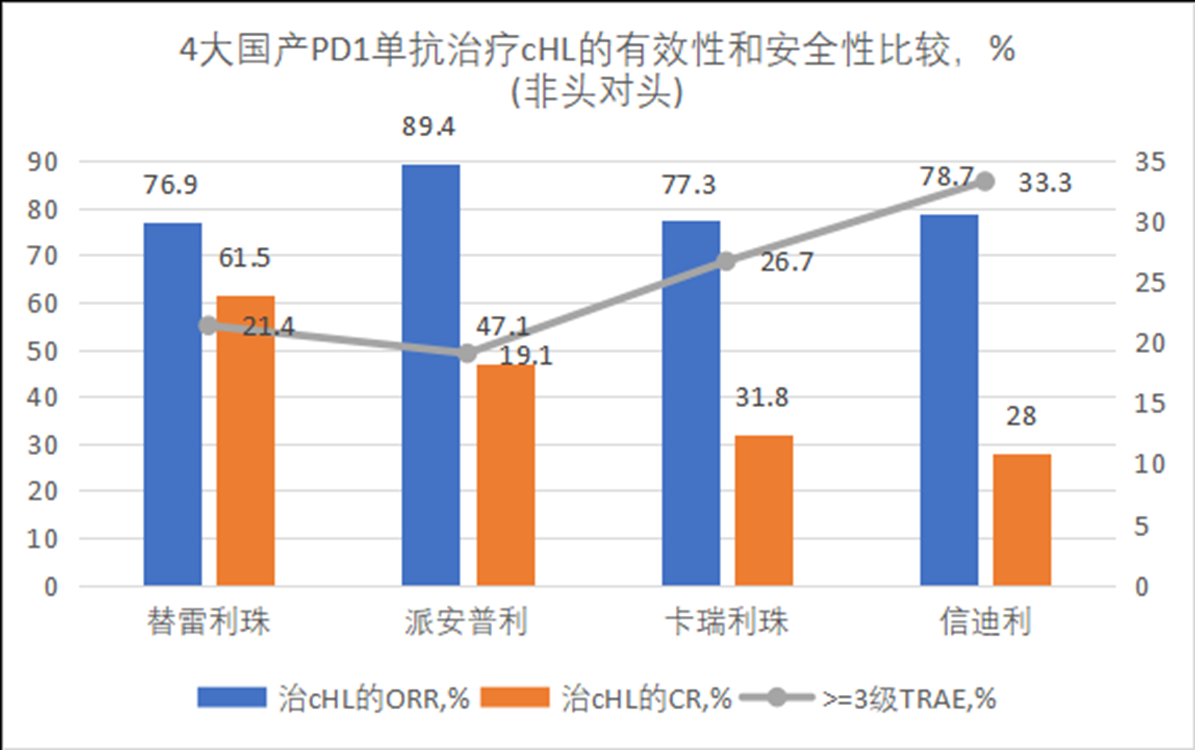
上图是4款国产PD1单抗治疗cHL披露的有效率和安全性数据,对Fc端改造更充分的替雷利珠、派安普利,它们的CR率明显超出卡瑞利珠和信迪利,与此同时,>=3级TRAE却明显更低。虽然不是头对头数据,而且只是一个小适应症的数据,但仍然展现了一定的趋势,让我们去思考和重视FC改造对PD1单抗性能的影响。而泽布替尼与奥布替尼的比较也类似,虽然没有头对头数据,但可比临床数据仍然展现了奥布替尼综合性能或优于泽布替尼的可能性。
不探讨相关公司的可投性问题,仅就创新药的竞争特性来说,中国市场与美国市场有较大区别。按我们的理解,差异主要还是在“美国医生在新药的选择上会更规范,而国内医生会更灵活”。
在美国新药市场,即使已有数据在几年前已经明确提示了阿卡替尼、泽布替尼相比伊布替尼的性能优势,但后者只到真正用头对头大3期证明了相比伊布替尼的显著优势,终端市场才开始展现明显的替代趋势。同样的,即使已有数据已经证明某个新药在某个新拓展适应症的显著获益,但只要还未完全获批,就很难通过超适应症去推广应用。
在中国新药市场,即使没有头对头大3期证明优劣,医生依然可能会基于自己对数据的理解而形成自己的性能差异判断;即使新适应症尚未真正获得药监局获批,医生依然可能会根据已有的数据去推进off-lable使用。从某一角度来说,这不够规范,可能会增加潜在的医疗风险;但从另一个角度来说,新药之间有更大性能优势的产品互相替代起来也更为灵活,增加了终端市场的活力。
性能优势,不一定非得要头对头大3期才被认可;新适应症,不一定非得药监正式获批才能使用。国内医生在用药上的这种灵活性,对性能不占优的产品来说,意味着更大的竞争压力;对性能占优的产品来说,意味着更多的拓展可能。如果这是国内新药领域的普遍现象的话,那不只是PD1,在分析其它新药放量节奏时可能也要需要注意这其中的差异。
