(原标题:ODAC决议10:2限制PD-1在CPS<1 HER2阴性一线胃癌应用,利好国产双抗)
就在昨晚的FDA肿瘤药物咨询委员会(ODAC)审评会议上,ODAC专家委员会以以10:2的投票结果反对PD-1抑制剂一线治疗PD-L1阴性(CPS<1)、HER2阴性、微卫星稳定型(MSS)胃(G)/胃食管交界处(GEJ)腺癌。以11:1的投票结果反对PD-1抑制剂一线治疗PD-L1阴性(CPS <1)、不可切除性或转移性食管鳞状细胞癌(ESCC)。
但结合数据分析,PD-1/CTLA-4双抗卡度尼利相比众多PD-1单抗差异化优势非常突出。卡度尼利在PD-L1阴性(CPS<1)人群的疗效优势,这是它不同于PD-1,真正从临床价值上实现晚期胃癌全人群覆盖的关键。
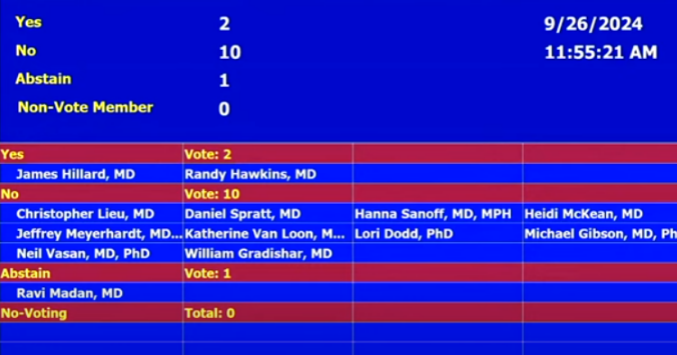
在胃癌领域,FDA ODAC这一审议涉及被CDE和FDA批准HER2阴性胃癌全人群的O药和K药,以及替雷利珠单抗的国内TAP≥5%适应症,替雷利珠单抗这一适应症在FDA审批中。梳理一线HER2阴性胃癌数据,不难发现,这一结果利于国产双抗PD-1/CLA-4一线胃癌适应症。
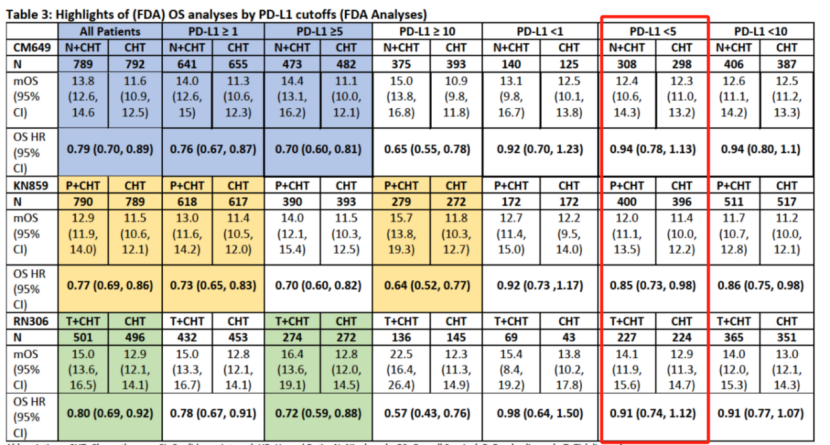
首先,我们可以看到,在整体晚期胃癌人群一线治疗中,与单纯化疗方案相比,PD-1抑制剂的加入通常能使患者的死亡风险降低约20%(OS HR 0.77~0.8),但卡度尼利单抗的这一数值达到了38%(OS HR 0.62)。
PD-L1表达是晚期胃癌一线治疗效果的正向预测性生物标志物,即PD-L1表达越高,疗效越好。如下图所示,在各个PD-L1表达亚组人群中,卡度尼利单抗的表现都非常好,都远优于K药、O药,卡度尼利的加入对死亡风险的降低都高于K药和O药13%~23%。
另外,最值得关注的PD-L1阴性和人群中,可以看到,卡度尼利无论相比K药还是O药在数值上都领先一大截。在CPS<1人群中,O药和K药加入化疗,仅相对降低8%的死亡风险(HR 0.92);但卡度尼利的加入在死亡风险的降低上达到23%(HR 0.77)。
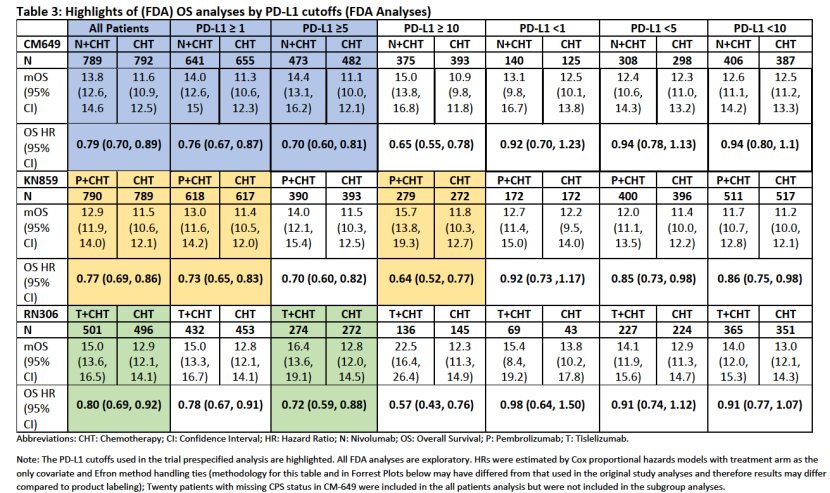
根据FDA的统计分析,O药、K药和T药在PD-L1<1/5/10人群获益有限,HR接近0.9~1,几乎较单纯化疗未进一步获益。实际上在去年,FDA已基于KEYONOTE-811研究中K药(帕博利珠单抗)加入曲妥珠单抗+化疗未进一步改善PD-L1阴性人群OS限制了该方案对于PD-L1阴性(CPS<1)的HER2阴性人群的适应症。本次ODAC会议再次体现了,监管方对在晚期胃癌中基于PD-L1表达用药的重视。
PD-L1低表达人群占比高,但现有PD-1疗效低,基于PD-L1表达用药是大势所趋。以我国为例,胃癌中PD-L1低表达人群(PD-L1CPS<5) 就占比 50.7%,PD-L1阴性人群(CPS<1)占比38%,也就是有一半人晚期胃癌是PD-L1低表达的。在免疫治疗药物普遍在PD-L1高表达疗效均不错的情况下,在低表达人群中的具有实际疗效才能真正体现药物差异化优势,卡度尼利做到了。
在卡度尼利单抗之前,HER2阴性胃癌一线治疗,O药(CheckMate-649),K药(KEYNOTE-859)、替雷利珠单抗(RATIONALE-305),信迪利单抗(ORINET-16),还有基石的PD-L1舒格利单抗(GEMSTONE-303研究)都已在国内获批。
其中替雷利珠单抗(TAP≥5%)和舒格利单抗(CPS≥5)获批的适应症批准受限于PD-L1表达,不能用于低表达人群。而K药、O药虽然在FDA和CDE均获批了全人群适应症,也就是不论PD-L1表达水平,但CSCO指南和NCCN指南、ASCO指南均只给了PD-L1高表达人群的以最高推荐,可见临床医生在实际临床场景中更为慎重的态度。
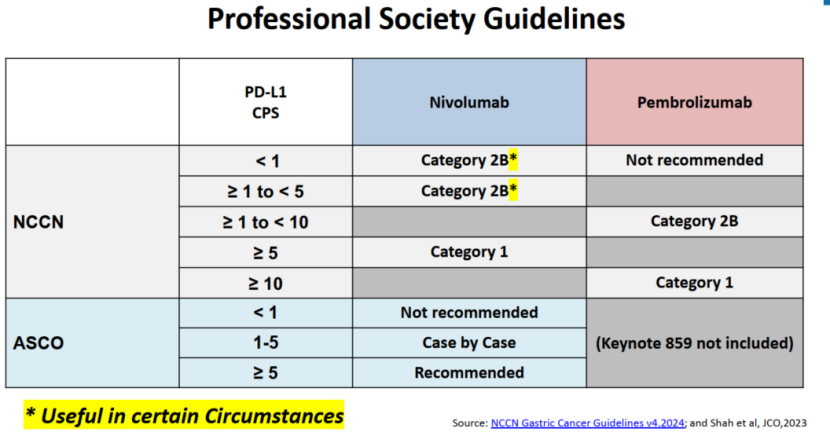
其实早在2022年中国医生发表在JCO的文章就指出(Zhao JJ,JCO . 2022),跟单纯化疗比,免疫检查点抑制剂的加入,并不能给PD-L1低表达胃癌人群带来OS和PFS显著获益。这也早于FDA的9月ODAC会议。
如前文所述,O药和K药以及替雷利珠单抗对于PD-L1低表达的人群疗效有限。
01 O药在CPS≥5人群疗效比较可观,但CPS<5时获益有限。
O药一线胃癌关键研究CheckMate-649中,在PD-L1阴性患者(CPS<1),纳武利尤单抗的加入仅使死亡风险降低了8%(HR 0.92),OS仅延长了0.6个月。在PD-L1低表达(CPS<5)人群中也仅降低6%且OS仅延长了0.1个月(12.4 个月vs 12.3个月)。虽然ITT人群的OS在统计学上具有显著性(HR=0.79),但O药仅在CPS≥5的PD-L1高表达人群中对死亡风险的降低达到30%(HR=0.7)。
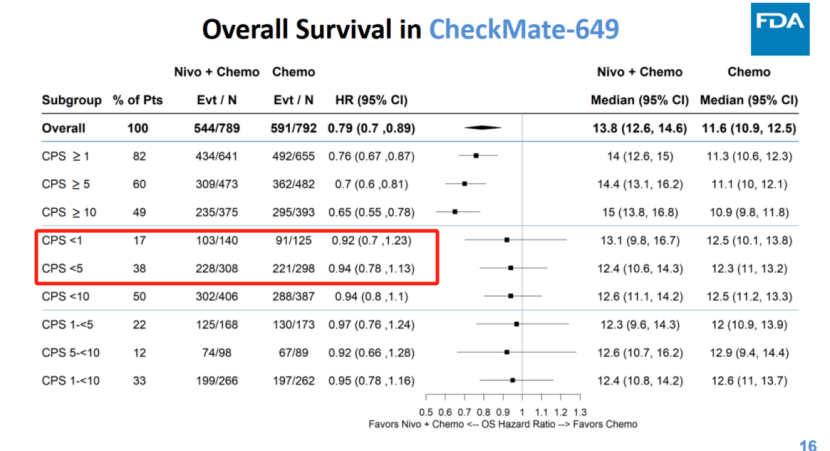
CheckMate-649 OS分层
02 K药在CPS≥10人群的疗效数据是比较可观的,但<10有限。
FDA去年11月基于KEYNOTE-859试验的结果,批准了K药与化疗的联合方案,且不受PD-L1表达的限制。虽然帕博利珠单抗的加入将死亡风险降低了22%(HR=0.78),但OS仅提高了1.4个月。
在PD-L1阴性(CPS<1)人群中,死亡风险降低幅度也仅为8%,HR值0.92。CPS<10的HR数值为0.86,HR边界非常接近1为0.983已经非常接近1了,K药带来的获益极其有限。从亚组看,K药的加入,仅在CPS≥10人群中,HR做到了0.64,降低死亡风险超过20%,达到34%。
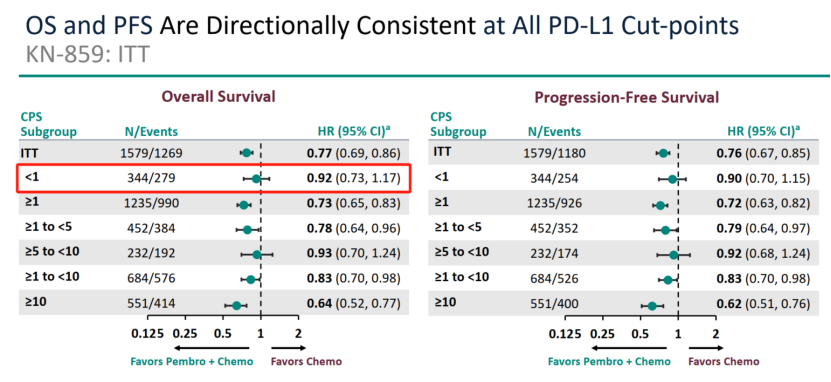
KEYNOTE-859 OS分层
除了百时美施贵宝的纳武利尤单抗和默沙东的帕博利珠单抗,百济神州替雷利珠单抗的PD-L1阴性患者受益也一样有限。
03 替雷利珠单抗在TAP≥5%人群的数据可观,但<5%获益一般。
在替雷利珠单抗一线胃癌3期RATIONALE-305试验中,在PD-L1阳性患者(TAP≥5%)中,替雷利珠单抗联合化疗在最终分析中使死亡风险降低了29%(OS HR 0.71)。在PD-L1阴性(TAP<5%)患者中,与单独化疗相比,替雷利珠单抗+化疗仅降低8%的死亡风险(OS HR 0.92 95%CI 0.75-1.13),这个获益非常有限。
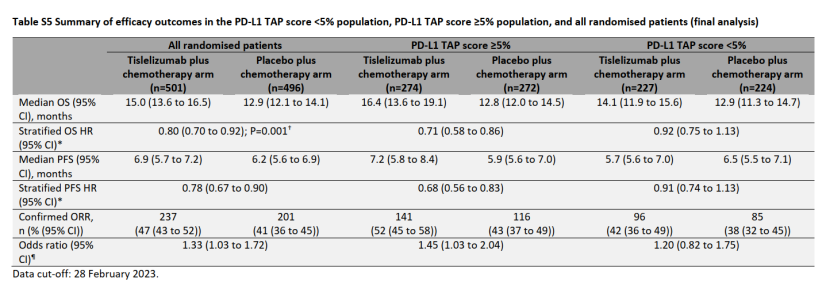
在所有入组患者中,死亡风险降低20%达到了统计学显著性。换算为CPS表达来看,替雷利珠单抗在CPS≥1人群的HR 为0.78,边界在0.67-0.91,险在1的边界里。
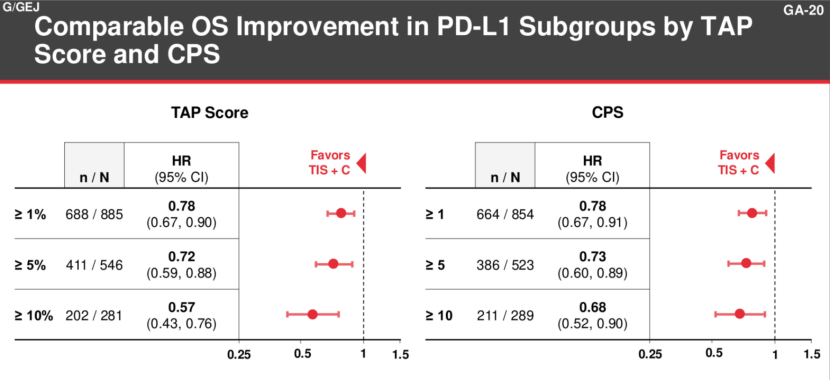
04 卡度尼利无论在CPS<1,还是<5,≥5均较好,优于K药、O药和替雷利珠。
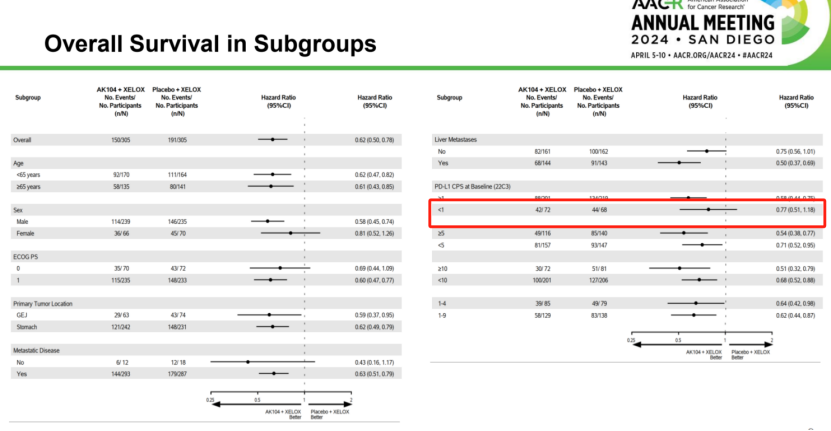
但在PD-1/CTLA-4双抗卡度尼利单抗一线胃癌3期COMPASSION-15研究中,在全人群中,卡度尼利的加入延长了4.2个月的OS,相对降低了38%的死亡风险,是所有疗法中生存期差值绝对值最高的。
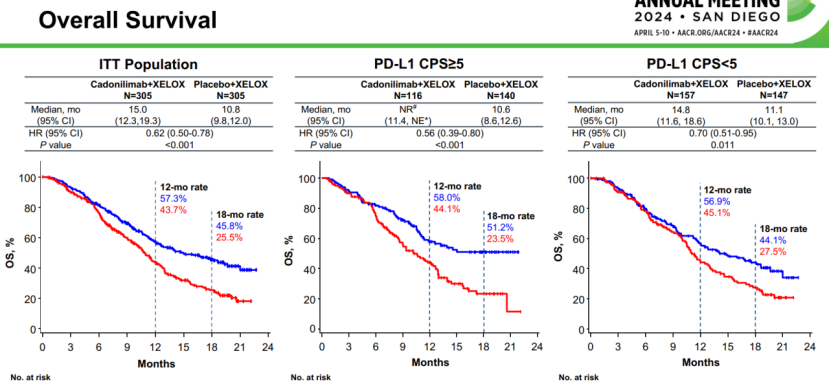
卡度尼利在低表达(CPS<5)人群的死亡风险的相对降低达到了30%,OS延长了3.7个月。而根据FDA统计,O药在这一组的数值表现分别为6%和0.1个月,在K药是15%和0.6个月,在替雷利珠单抗(TAP<5%)是9%和1.2个月。
在CPS<1人群中,O药和K药加入化疗,仅相对降低8%的死亡风险(HR 0.92);但卡度尼利的加入在死亡风险的降低上达到23%(HR 0.77)。
除了PD-L1低表达胃癌中,卡度尼利单抗疗效突出,卡度尼利头对头替雷利珠单抗一线治疗PD-L1阴性肺癌的三期研究也在开展,由此在肺癌阴性人群的疗效非常值得期待。
除了PD-1原发响应不佳的PD-L1阴性人群,康方还布局了卡度尼利在IO继续耐药人群的临床开发,联合抗血管药物二线治疗PD-1/L1经治的胃癌三期也在开展。
整体上,卡度尼利单抗是克服当前免疫治疗局限的下一代值得关注的免疫药物,也展出了下一代免疫基石药物的潜力。在国内外PD-1/L1抑制剂集体“乏力”的情形下,卡度尼利单抗的全球价值也再度引起重视,而FDA对HER2阴性胃癌的审批结果也值得继续关注,这将对全球晚期胃癌治疗带来巨大影响。$康方生物(09926)$ $百济神州(06160)$ $百济神州(06160)$










