(原标题:【药海听涛】东邪西毒还是东成西就:减肥的明天是siRNA吗?)
在GLP-1席卷八荒的力量下,医药企业手头要是没有能沾上减肥的资产,似乎就快要不容于时代。于是,卷完单靶卷双/多靶,卷完注射卷口服,卷完降幅卷降速,卷完用药卷维持,卷完减重卷增肌……如今终于卷到了天生适合长效给药治疗代谢疾病的siRNA头上。
有卧龙必有凤雏,这个领域的两家龙头企业$阿里拉姆制药(ALNY)$ 与$Arrowhead制药(ARWR)$ ,目前浮上水面的信号通路上的两个靶点INHBE与ALK7,各有一些早期进展、又仍有一堆不确定的问题,恰好形成了2x2的选项。我们不妨结合最近披露的结果,来看看这里面谁是《东邪西毒》、谁是《东成西就》?
(注:正因为这两部巨作的交织、争议、模糊、且都很伟大,故作此喻)
0. INHBE-ALK7信号通路
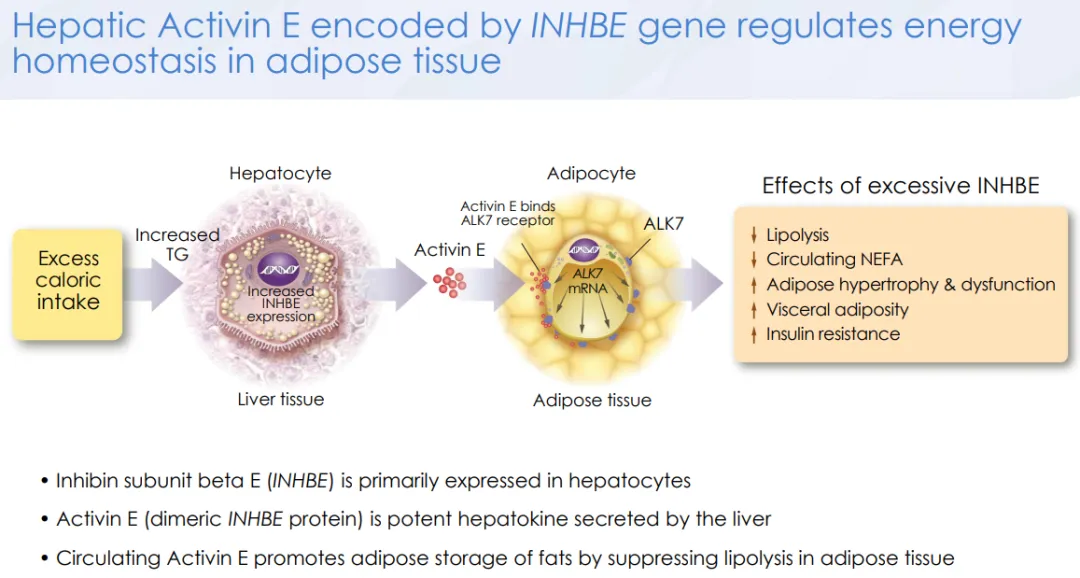
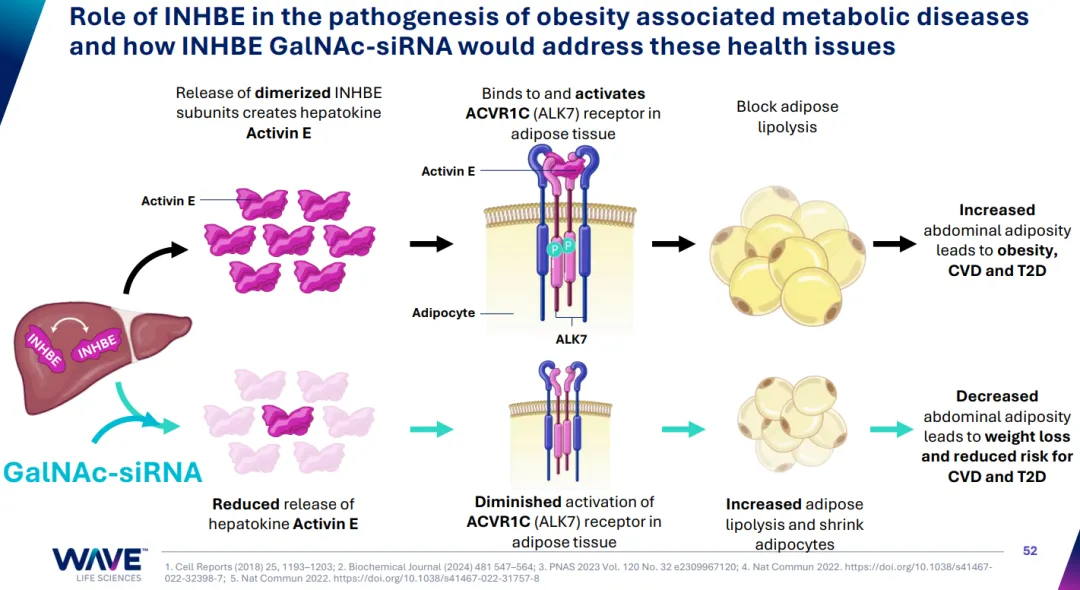
INHBE基因(Inhibin Subunit β E)主要在肝细胞中表达,过多热疗摄入导致的甘油三酯升高会显著上调INHBE的表达,其编码的蛋白通过二聚化形成一种TGFβ超家族的配体Activin E,进而激活表达于脂肪组织(特别是白色脂肪细胞)的受体ALK7(也称ACVR1c),二者结合后可激活下游的Smad2/3信号,导致脂代谢下降、脂肪堆积、胰岛素抵抗等恶性循环。
网页链接
网页链接
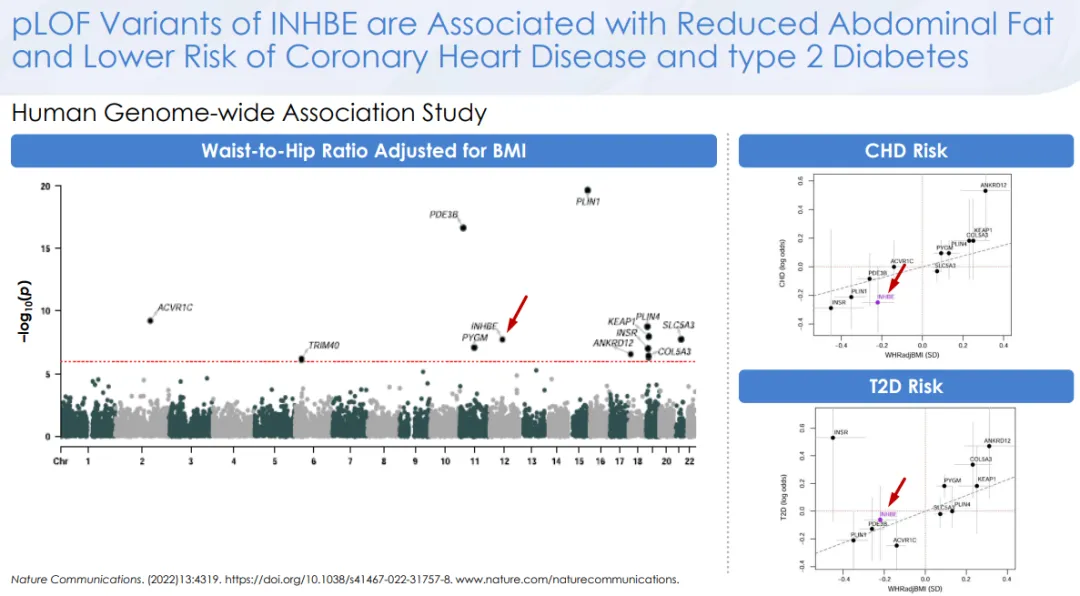
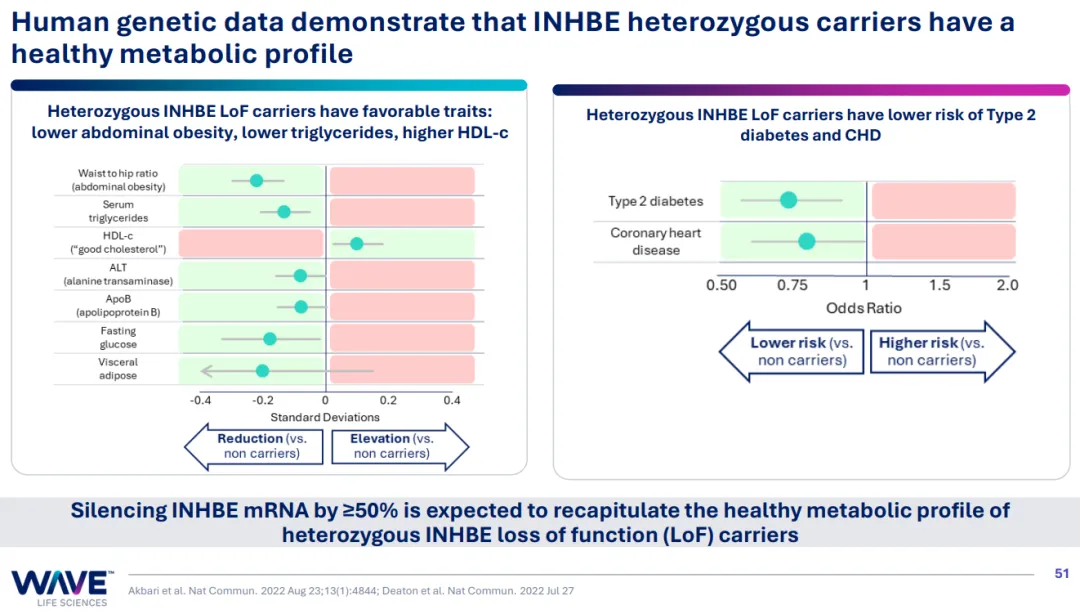
这条信号通路对于肥胖乃至心血管疾病的作用,已经有一系列遗传学证据,而靶向肝细胞和脂肪细胞的小核酸递送工具的成熟又提供了手段,因此靶向敲降INHBE和ALK7的siRNA药物就成了减肥大热背景下的显学。
1. INHBE siRNA
由于INHBE主要表达于肝细胞,正好发挥GalNAc靶向肝的能力,所以成为各家siRNA企业进入减肥领域的首选。
1)ARO-INHBE
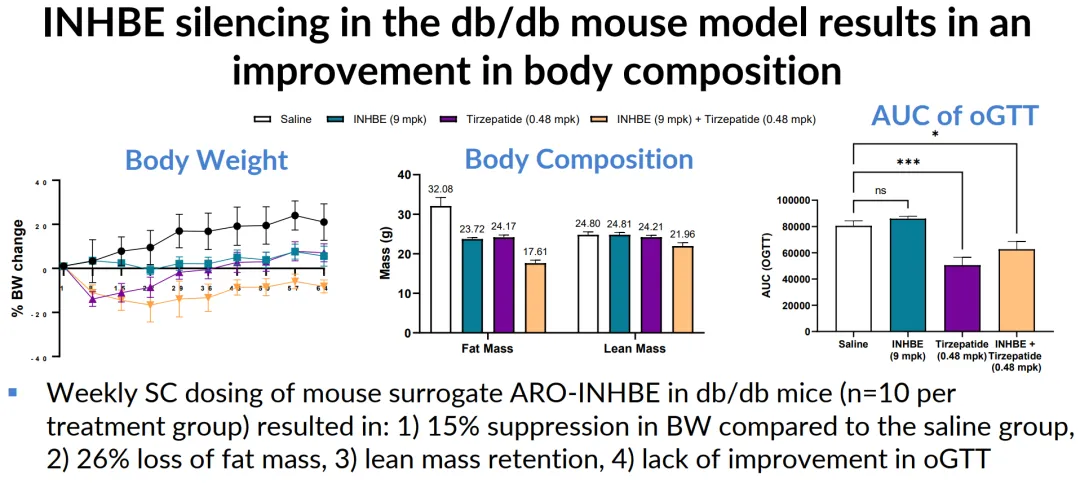
Arrowhead率先领跑,早在去年ADA就公布了ARO-INHBE的临床前研究结果。在DIO小鼠模型中,9mpk的INHBE能实现约94%幅度的mRNA敲降,但减重效果远远不如Tirzepatide。(此外,有一说一后来Arrowhead在R&D webinar的披露略显鸡贼,只展示ARO-INHBE而刻意把Tirzepatide对照组全都拿掉,下图上半部分是6月ADA版本、下半部分是8月Webinar版本,在此对比,下文不再重复列出。)
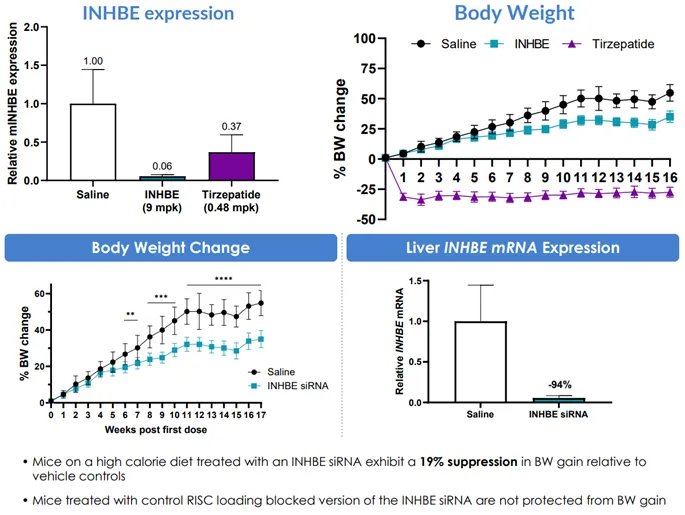
网页链接
从体重变化的构成来看,确实验证了INHBE调控脂代谢的作用,脂肪重量降低26%、肌肉重量没有下降甚至还有上升,与Tirzepatide同时减脂肪和肌肉截然不同,毕竟后者是以抑制食欲为主要的减重方式。不过坦率说,这样的减重幅度就算有不掉肌肉的优势,几乎注定了单药很难有临床价值。
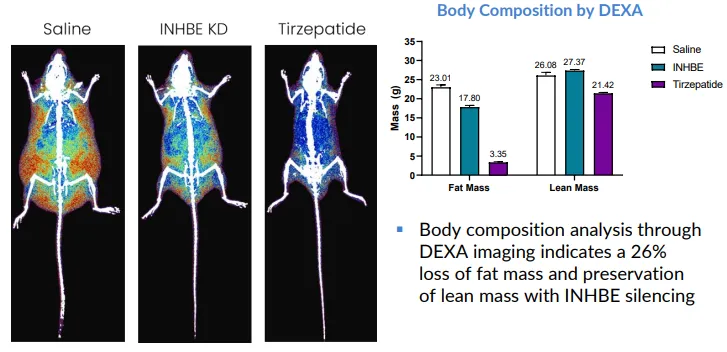
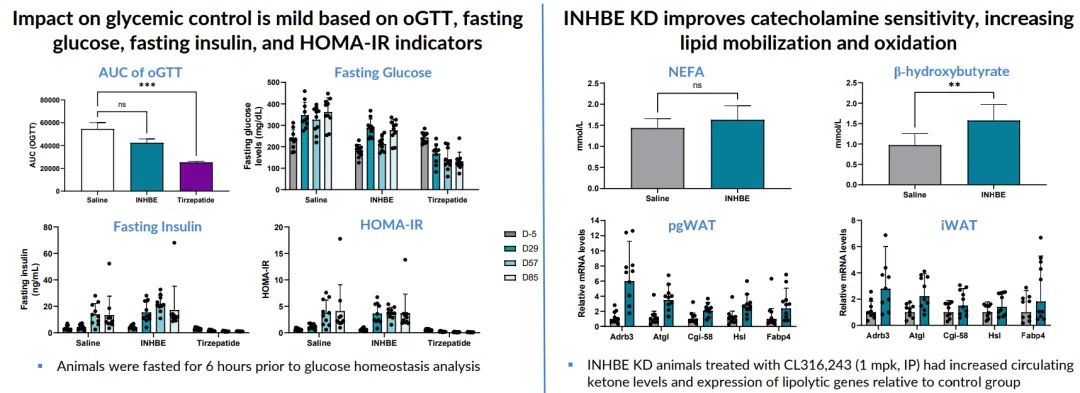
除了减重,ARO-INHBE单药对于血糖调控也显著弱于Tirzepatide,更多还是作用于脂代谢。
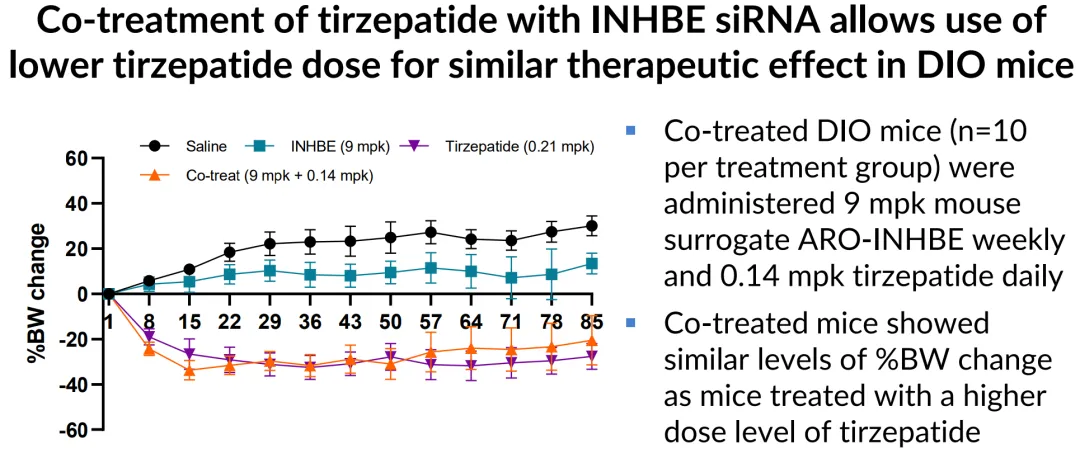
至于联用方案,在DIO小鼠模型中,9mpk QW ARO-INHBE与低剂量0.14mpk QD Tirzepatide的联用,减重效果也只与高剂量0.21mpk QD Tirzepatide相当;在db/db小鼠模型中,每周9mpk ARO-INHBE+0.48mpk Tirzepatide确实比两个单药持续减重效果更好,提供了额外约15%的减重幅度,其中脂肪减重幅度约26%、但肌肉重量也比单药有额外下降,而在血糖控制方面依然显示不出协同性。
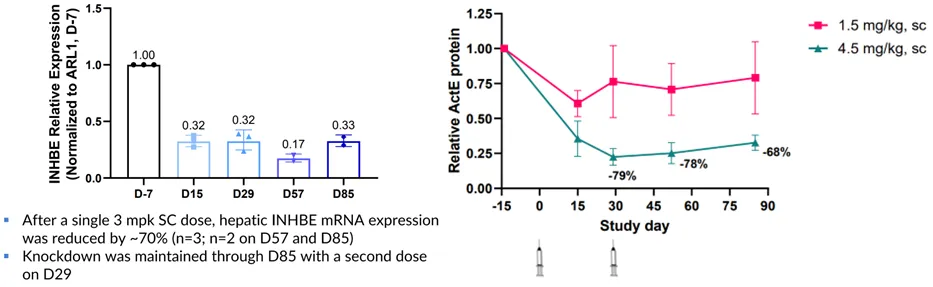
最后是在食蟹猴体内的敲降效率,在高剂量4.5mpk一针后大约敲降70%,在4周后第二针最多敲降到80%,至12周保持在大约70%水平。同样微妙的是,前后两次Arrowhead选择将中剂量3mpk和高低剂量1.5/4.5mpk分开披露(下图左右部分),而结合在一起可以发现,剂量从1.5到3敲降效率显著提升,而从3到4.5则并无显著提升。
在2024年底ARO-INHBE的临床1/2a期已经启动,第一部分针对肥胖受试者进行SAD和MAD剂量爬坡,第二部分则针对肥胖±T2D患者进行联用Tirzepatide的拓展试验。

2)WVE-007
紧跟在Arrowhead之后的反倒是$Wave Life Sciences(WVE)$ ,公司去年10月底R&D Day公布了WVE-007的临床前结果。
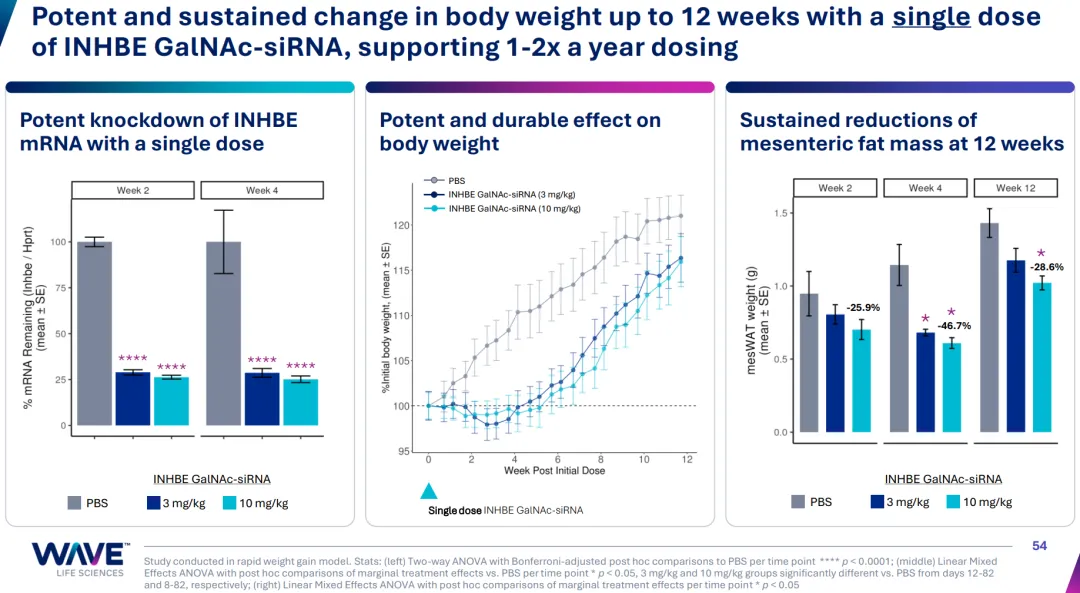
在DIO小鼠中,3mpk和10mpk的INHBE敲降效率都只能到75%左右,这远低于ARO-INHBE的94%;反而单次给药后就能带来显著体重降幅、4周后高剂量甚至能相对减重达到46.7%、其中脂肪减重40%且肌肉重量基本维持,这显著优于ARO-INHBE(体重绝对值完全看不到下降,相对减重也就19%、其中脂肪减重26%)。这使得WVE-007看上去至少有可能单药用于减重。

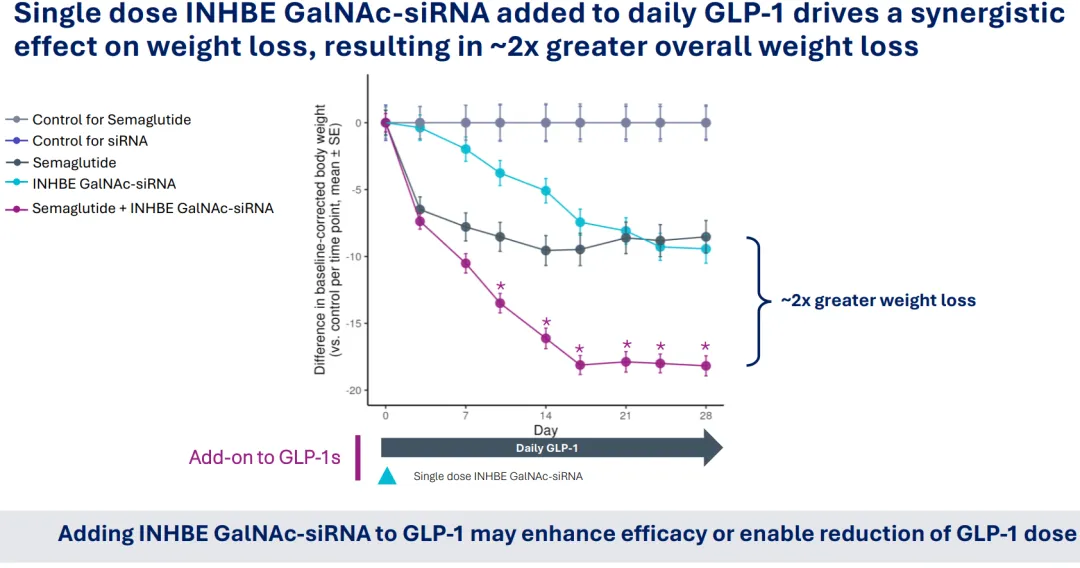
在与GLP-1联用的探索方面,WVE-007也有比ARO-INHBE相对更清晰的证据,一方面是单次给药作为Semaglutide的add-on能相比单药带来2倍的减重幅度扩大(4周从约9%到18%),另一方面是作为Semaglutide停药后的维持治疗能显著减少体重反弹。
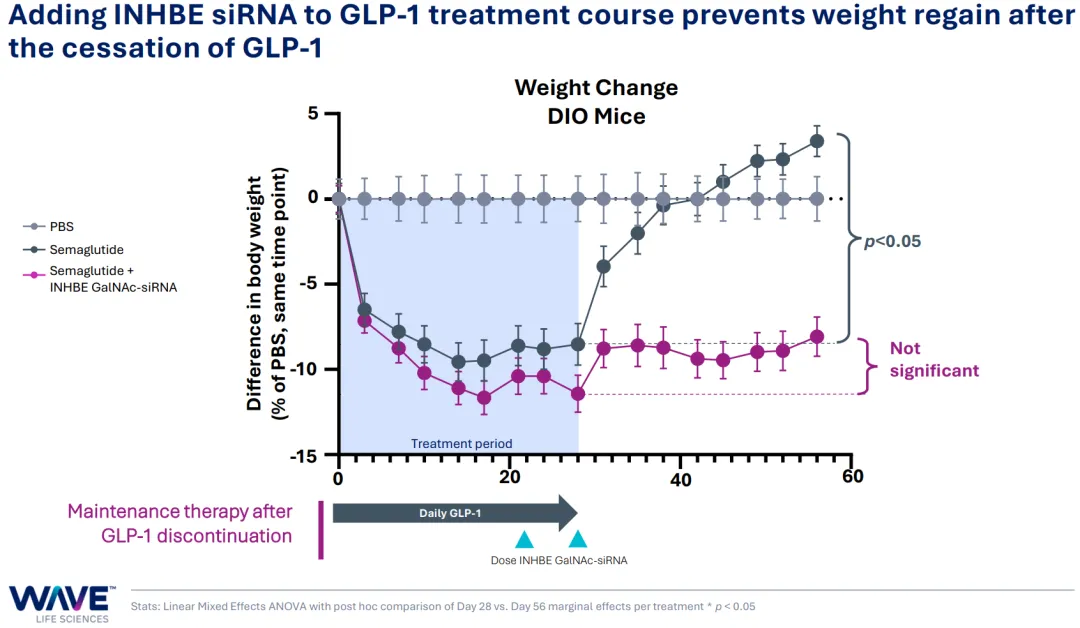
WVE-007的IND申请于2024年12月提交,一期临床将于2025年一季度启动。
3)ALN-INHBE
Alnylam在INHBE的动作显著偏慢(后文详述他们明显更偏向ALK7),虽然2023年R&D Day就提及了这个靶点,直至2025年2月最新的R&D Day才又公布了一些临床前结果。
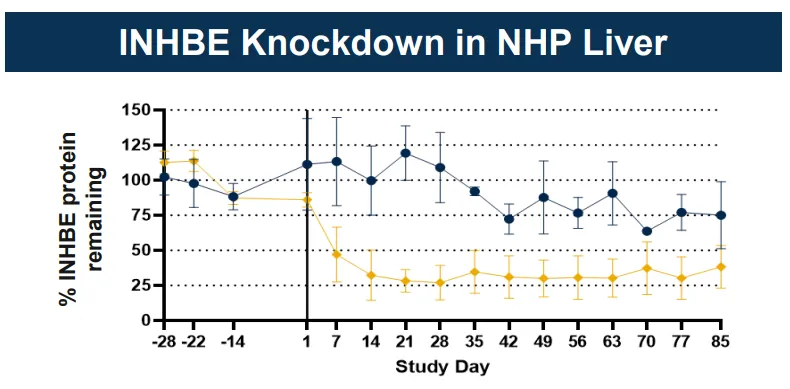
在敲降效率上,ALN-INHBE也是在75%左右,与WVE-007相近、而都低于ARO-INHBE。
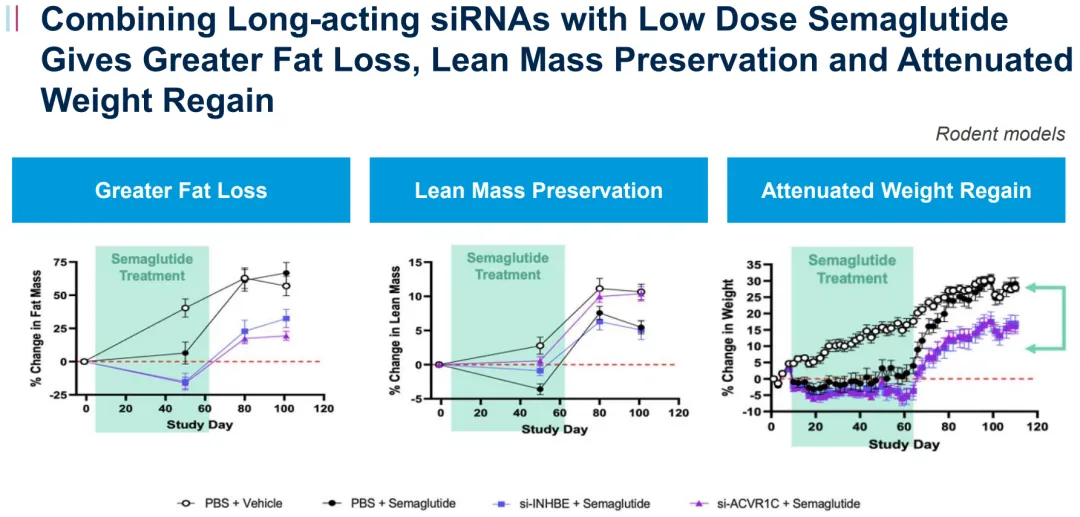
在减重用药的策略上,Alnylam似乎比较直接地选择作为GLP-1停药后的维持策略(是不是就可以反推对于单药的临床价值不抱太大信心),在小鼠模型证明ALN-INHBE与低剂量Semaglutide联用,能有效降低脂肪重量、维持肌肉重量、从而最终减缓Semaglutide停药后的体重反弹。
2. ALK7 siRNA及脂肪递送系统
与INHBE不同,ALK7受体主要表达于脂肪细胞,所以ALK7 siRNA首先需要解决小核酸的脂肪递送问题。
1)ARO-ALK7与TRiM系统
Arrowhead的递送思路是用两种脂质配体结合在siRNA的正义链上,来实现靶向皮下和内脏脂肪的递送。
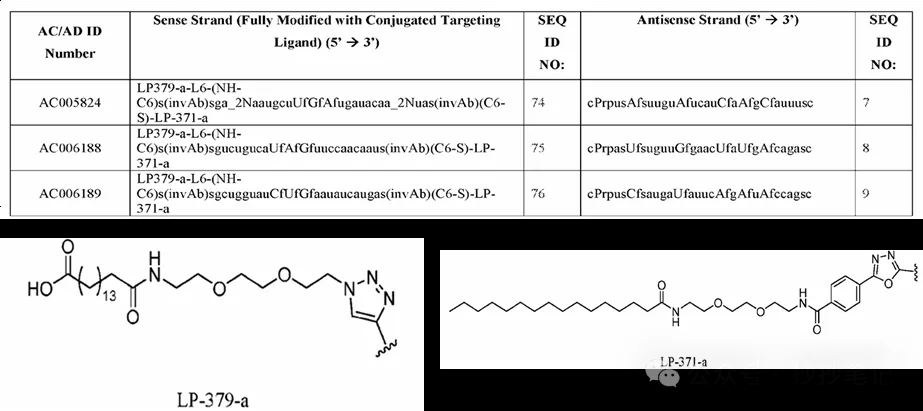
TRiM在两种脂肪组织的递送效率都得到一定的验证,包括皮下和静脉注射剂型,都能实现深度和持久的敲降,且递送的组织特异性较好。
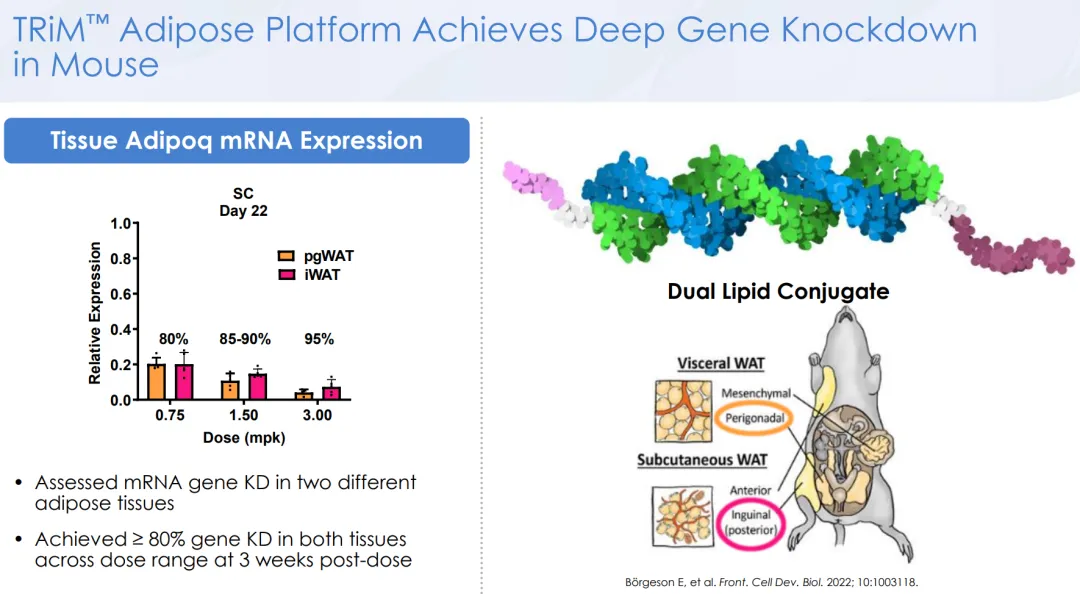
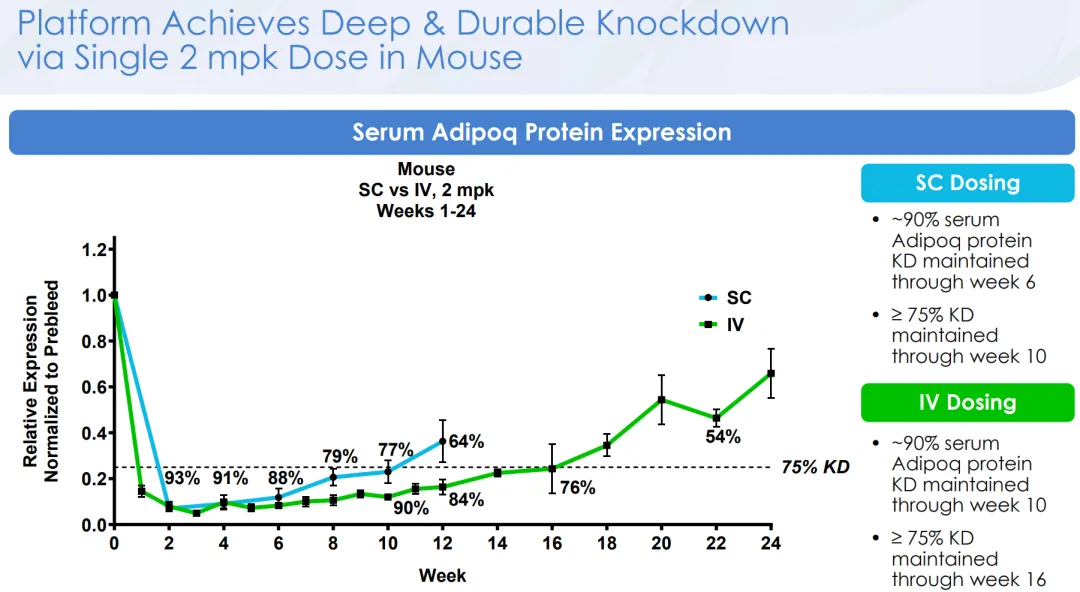
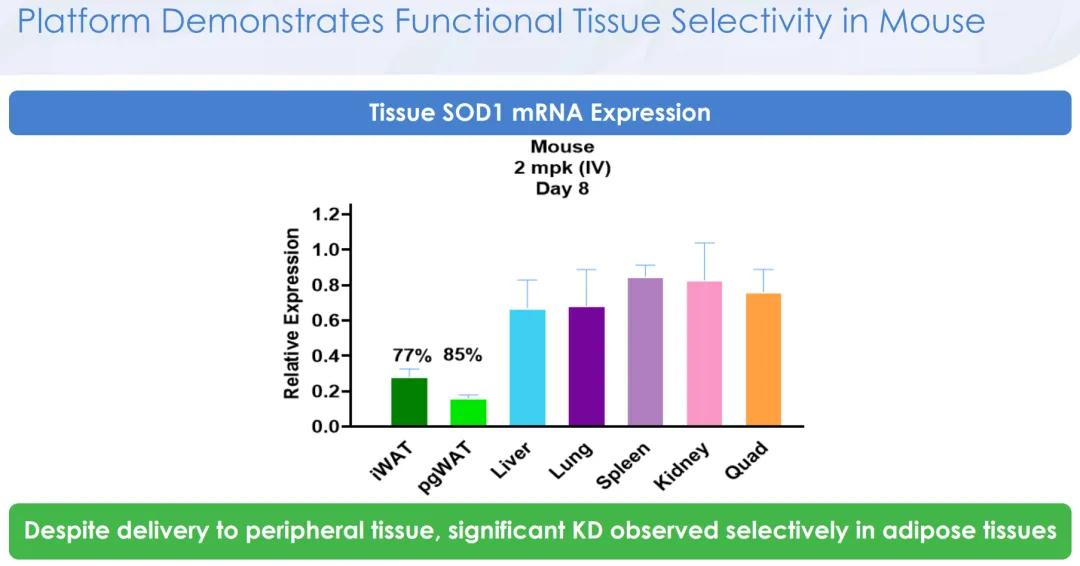
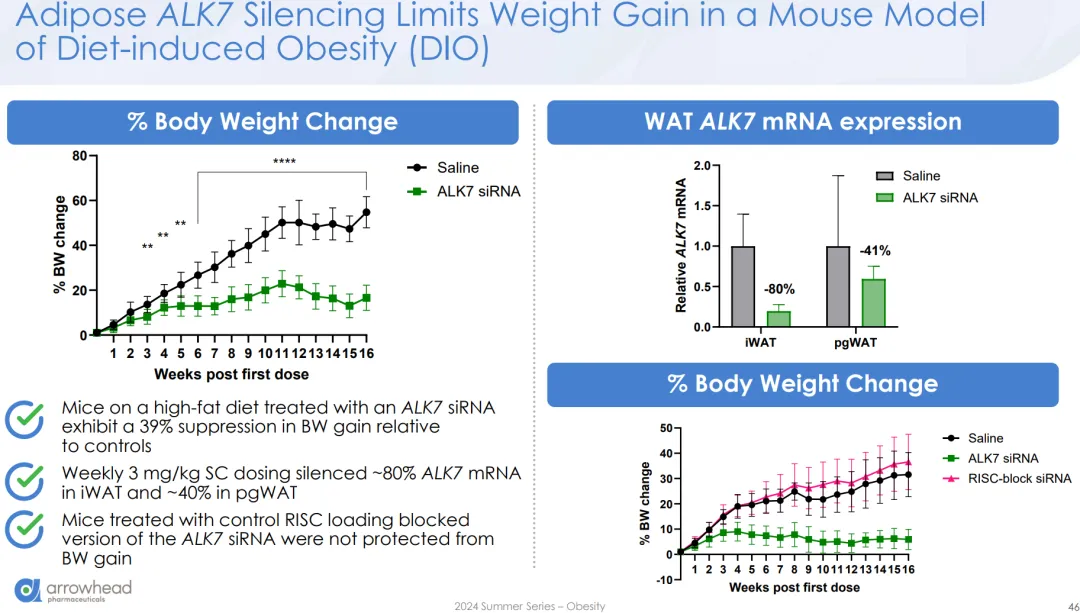
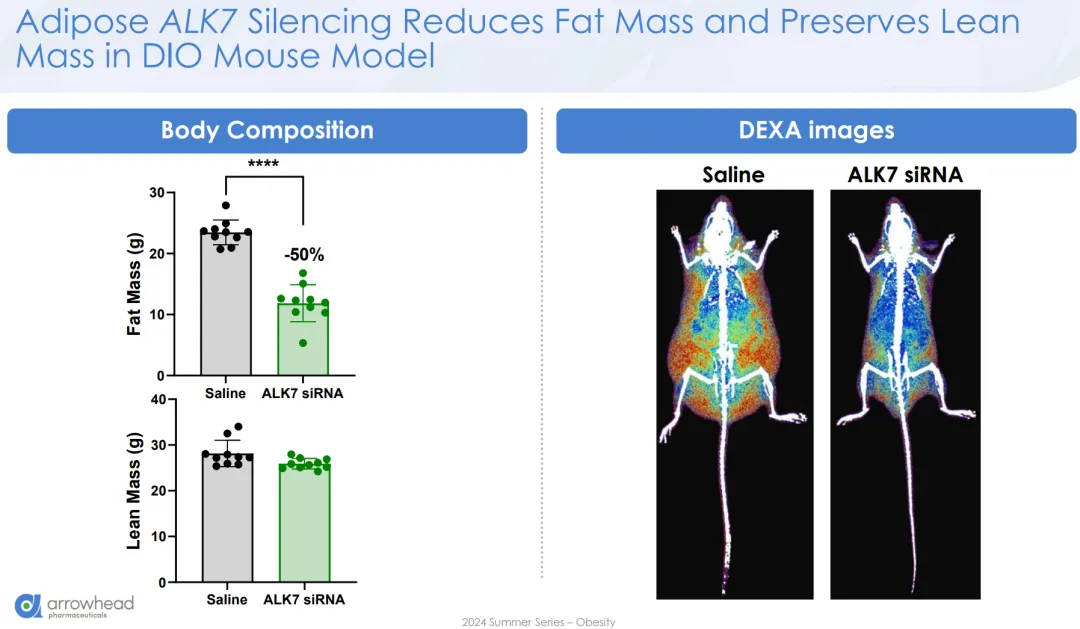
具体到ARO-ALK7,在DIO小鼠模型中,3mpk QW皮下注射的ARO-ALK7,针对皮下和内脏脂肪的敲降效率分别为80%和41%(后者还是明显偏低了);相比安慰剂能带来约39%的体重降幅,其中脂肪重量降低约50%、肌肉重量基本维持不变,这都比ARO-INHBE单药表现更好。
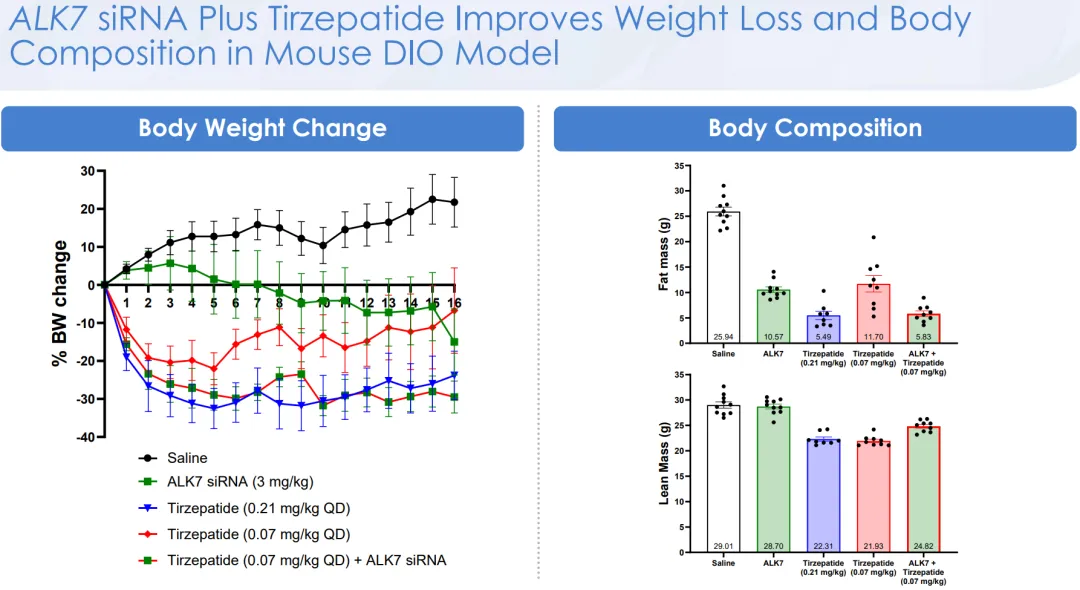
在与Tirzepatide对比中,3mpk QW ARO-ALK7与低剂量0.07mpk QD Tirzepatide联用的减重幅度与高剂量0.21mpk QD Tirzepatide相当,而ARO-ALK7单药依然无法与Tirzepatide单药相比;在减重构成方面,ARO-ALK7+低剂量Tirzepatide联用能比单药提供额外约23%的脂肪重量下降(ARO-INHBE是约26%),但与高剂量Tirzepatide单药差距不大(这里Arrowhead在2025年2月的symposia里又单独把下图里的高剂量Tirzepatide组全删了)。
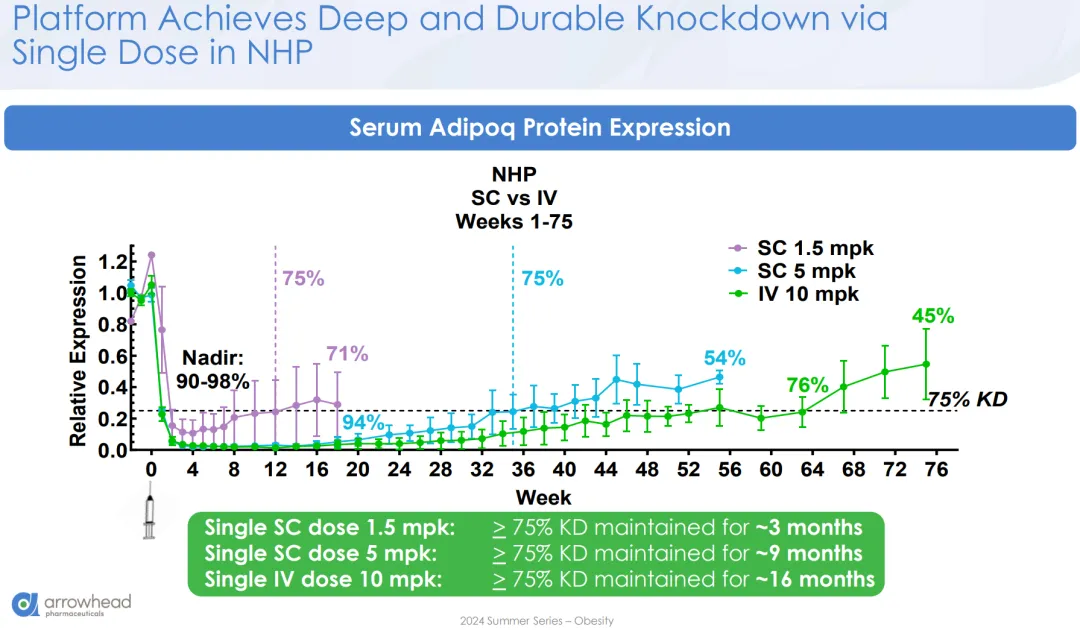
最后是食蟹猴体内的敲降效率,又出现了略微妙的披露(下图上半部分是2024年8月webinar版本、下半部分是2025年2月symposia版本),3mpk剂量最多敲降94%且至26周依然能维持在75%水平,1.5mpk剂量最多敲降91%且至20周就反弹到45%,咱也不知道后披露1.5mpk是否意味着公司在平衡有效性和安全性。

ARO-ALK7已经取得澳洲临床许可,2025年一季度将启动1/2a期临床,方案与ARO-INHBE类似。

2)ALN-2232与AdipoLigand1
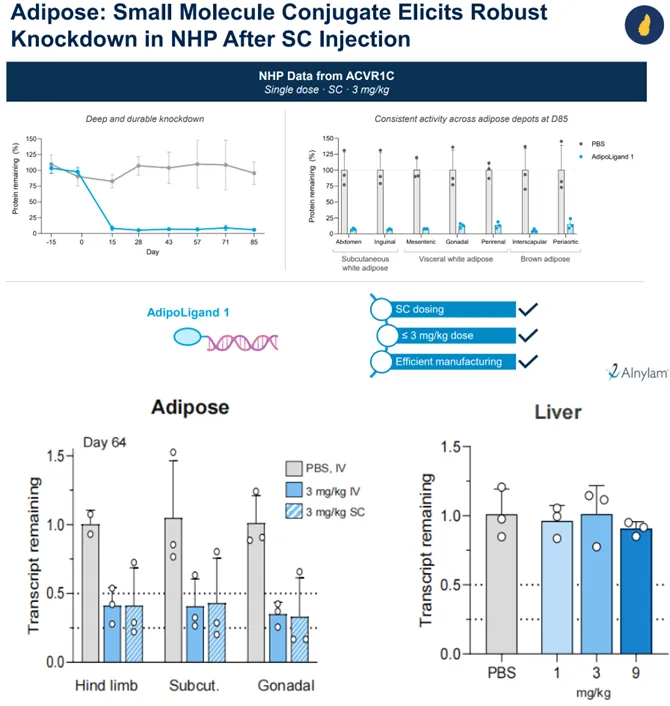
Alnylam在2025年2月最新的R&D Day首次正式披露其脂肪靶向递送系统,是利用一种与脂肪酸转运蛋白结合的小分子配体AdipoLigand1,在NHP单次皮下给药3mpk就可实现对ALK7的95%以上且持续的敲降,这明显优于2023年底披露的初级版本,看起来明显强于Arrowhead的TRiM(是否需要这样的敲降深度另当别论)。
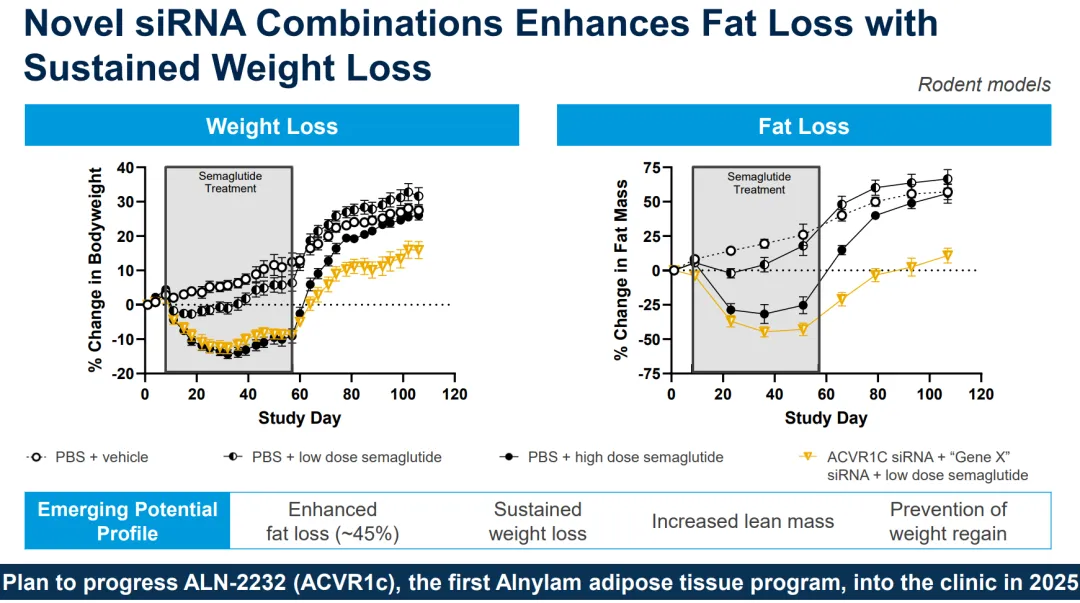
与上文ALN-INHBE类似,靶向ALK7的ALN-2232在减重上似乎基本放弃单药策略,而是更保守地选择与一个未披露靶点的Gene X siRNA以及低剂量Semaglutide联用,作为增强和维持治疗,该联用方案能提供约45%的额外脂肪减重、肌肉重量增加、维持减重幅度和减缓反弹。
ALN-2232目前仍在IND-enabling,但Alnylam明确将在2025年推进它作为公司首个靶向脂肪的管线进入临床。
整体而言,siRNA公司在减肥领域的格局远未到能看清的地步。
笨鸟先飞的Arrowhead率先进入临床阶段,然而递送和敲降效率/单药与联用GLP-1的药效/以及后续临床的策略,都仍有不尽如人意之处;Alnylam的进度偏慢,策略也偏保守,都并未将减肥摆在较高的优先级顺位;INHBE乘肝靶向GalNAc之便,但似乎药效和起效时间都并不占优;ALK7靶点看似没毛病,又毕竟牵扯全新的递送系统……
这种感觉,就好像“香肠嘴”与“盲剑客”,哪个角色更出彩谁又说得清呢?
