(原标题:普利制药亮了!海外收入大涨65%,今年13个美国ANDA高居全国药企第一)
深耕海内外市场30余年,普利制药始终坚持走“国际化战略”路线,锚定国内外双报、“仿创”结合的研发策略......近年来,公司研发管线喜讯频传:2024年至今以13个美国ANDA产品高居全国药企第一(并列),目前合计已获得36个美国ANDA;2021年以来在国内拿下21个新品(按产品名统计,下同),其中4个为首仿品种(含剂型首仿,下同);34个品种获批过评,包括首家品种11个,独家过评品种4个;2款在研1类新药加速推进,涉及FIC纳米创新药、高端造影剂等。
海外业务保持高增长,今年13个美国ANDA高居全国药企第一
作为医药制剂国际化先导企业,普利制药坚定不移地走国际化战略,充分发挥全球注册和高端国际化产能优势,在产品获批后积极推进产品上市,紧盯市场药品短缺机会,动态调整供应链,以加大力度开发国际空白市场。
据公司公告及官网显示,截至目前,普利制药已获得36个美国ANDA,剂型上以注射剂为主,占比超过80%;类别上看,抗细菌药和抗癫痫药均达5个及以上。其中,2024年至今,公司已收获13个美国ANDA,高居制剂出海全国药企第一位(并列),涉及阿奇霉素干混悬剂、注射用阿奇霉素、注射用盐酸多西环素等临床常用药。
普利制药获美国ANDA的产品
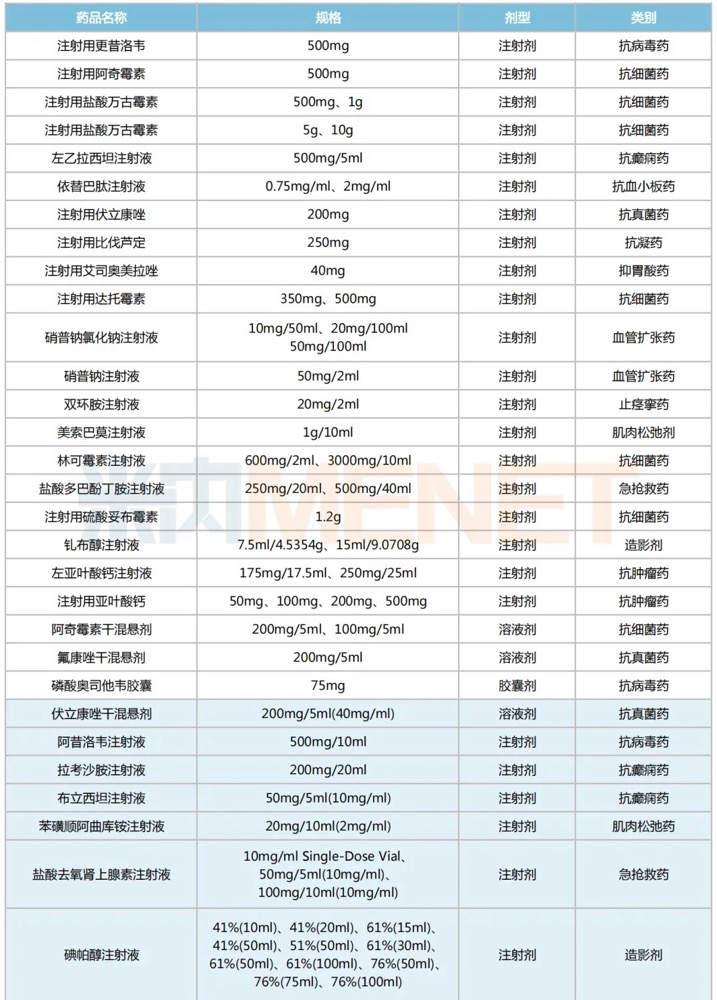
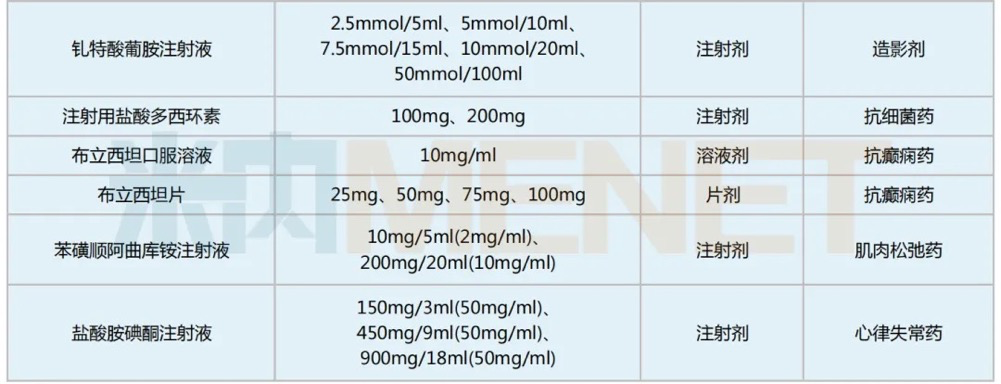
来源:公司公告及官网,米内网整理
注:高亮部分为2024年至今获批的美国ANDA
其中,阿奇霉素干混悬剂是一种大环内酯类抗菌药物,适用于成人和6个月及以上儿童患者的社区获得性肺炎、咽炎/扁桃体炎,以及成人慢性支气管炎的急性细菌感染性发作、急性细菌性鼻窦炎、尿道炎和宫颈炎等。
米内网美国FDA数据库显示,阿奇霉素干混悬剂是普利制药首款出口美国的干混悬剂,随后,氟康唑干混悬剂、伏立康唑干混悬剂于2023年9月和2024年1月分别获FDA批准上市。据悉,普利制药的阿奇霉素干混悬剂是国内首个且目前唯一获批上市的国产瓶装干混悬剂,其配备了精准给药器,最小给药剂量精确至0.1ml(2mg),与国内常规的袋装干混悬剂相比,进一步提高了儿童用药的精准度,以及药品的疗效和安全性。
普利制药获FDA批准的干混悬剂

来源:米内网美国FDA数据库
值得一提的是,普利制药的注射用阿奇霉素于2018年5月获批过评,是国内首个通过一致性评价的注射剂。依托引入国际先进的生产设备、优化生产工艺,加强质量管理体系建设等方式,该产品的药品质量和稳定性得到不断提高,目前已在海外13个国家及地区上市销售。随着阿奇霉素系列产品的相继出海,普利制药在国际抗感染药物市场的影响力也逐渐扩大。
注射用盐酸多西环素属于四环类抗生素,常用于治疗或预防已证实或强烈怀疑由易感细菌引起的感染,多种微生物(立克次体属、肺炎支原体等)、革兰氏阴性菌和革兰氏阳性菌引起的感染等。
根据普利制药公告,公司成功研发注射用盐酸多西环素仿制药后,分别递交美国和中国的仿制药注册申请,属于共线产品。目前,该产品已获FDA批准在美国上市,而在国内已提交上市申请在审。米内网数据显示,2023年中国三大终端六大市场(统计范围详见本文末)注射用盐酸多西环素销售额首破1亿元大关,同比涨幅达118.16%,市场潜力在释放。
近年来中国三大终端六大市场注射用盐酸多西环素销售趋势(单位:万元)
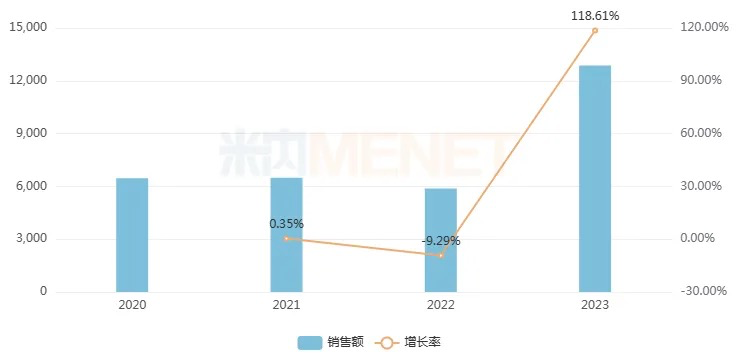
来源:米内网格局数据库
此外,普利制药还有7个美国ANDA正处审批阶段,产品包括:钆特醇注射液、泊沙康唑注射液、注射用替加环素、注射用环磷酰胺、注射用亚叶酸钙、注射用卡非佐米及托吡酯缓释胶囊,涵盖造影剂、抗感染、抗癫痫、抗肿瘤及免疫抑制剂等治疗领域。
“出海”步伐的提速,进一步推动公司海外业务收入的高增长。与去年同期相比,普利制药2024上半年的境外制剂销售收入实现+65%的增长率。这一成绩不仅展示了公司在国际市场上的强劲竞争力,也为公司的持续发展提供了坚实的支撑。
国内拿下21个新品,34个过评品种成绩亮眼
海外市场遍地开花的同时,普利制药继续秉持国内外双报的战略规划,近年来在国内获批的新品数逐年攀升,2021年、2022年、2023年及2024年至今分别有2个、5个、6个、8个新品获批上市。
2021年至今普利制药获批品种
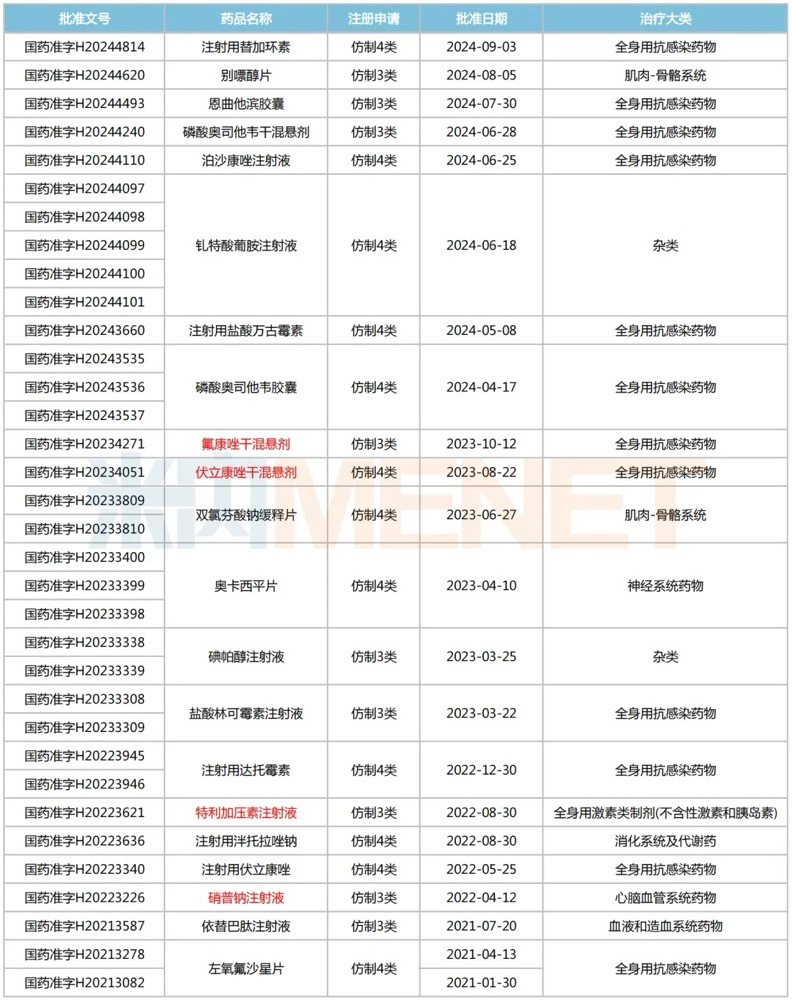
来源:米内网中国上市药品(MID)数据库
注:标红为首仿品种
新注册分类品种审评方面,2021年至今普利制药共有21个品种获批上市并视同过评,其中特利加压素注射液、硝普钠注射液、氟康唑干混悬剂及伏立康唑干混悬剂为首仿品种;另有24个品种提交上市申请在审,其中注射用卡非佐米、盐酸非索非那定口服混悬液、比拉斯汀片及左亚叶酸钙注射液暂无首仿获批。
普利制药过评/视同过评品种
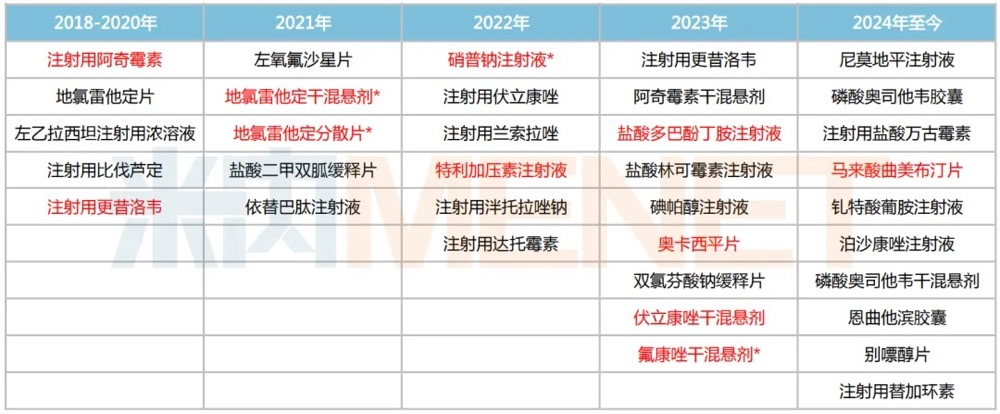
来源:米内网一致性评价进度数据库
注:标红为首家过评品种,带*为独家过评品种
存量品种一致性评价方面,普利制药已有11个品种先后过评,包括地氯雷他定干混悬剂、盐酸二甲双胍缓释片、注射用兰索拉唑、阿奇霉素干混悬剂、盐酸多巴酚丁胺注射液、注射用更昔洛韦、尼莫地平注射液、马来酸曲美布汀片等。
截至目前,普利制药已有34个品种通过/视同通过一致性评价,涵盖9个治疗大类,主要集中在全身用抗感染药物(15个)、消化系统及代谢药(4个)、呼吸系统用药(3个)、心脑血管系统药物(3个)。其中,11个品种为国内首家过评,4个品种为独家过评,分别是地氯雷他定干混悬剂、地氯雷他定分散片、硝普钠注射液及氟康唑干混悬剂。
聚焦“仿创”结合研发战略,2款1类新药蓄势待发
近年来,普利制药始终将创新研发置于战略核心,采取“仿创”相结合的研发思路,重点研发技术难度高、未来竞争格局好、具有差异化的仿制药产品,同时也在创新药领域进行了布局,特别是在抗肿瘤药和硼中子俘获疗法(BNCT)的硼药方面,以确保长期竞争力和市场地位。
米内网数据显示,目前普利制药有2款1类新药已进入/即将进入临床试验阶段,主要集中在抗肿瘤和免疫调节剂、造影剂两大治疗领域。
普利制药在研1类新药
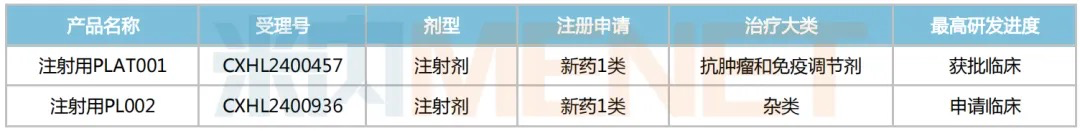
来源:米内网中国申报进度(MED)数据库
注射用PLAT001是普利制药研发的First-in-class纳米创新药,首次构建了γ-谷氨酰转肽酶(GGT)介导的电荷反转聚合物,并将其应用于抗肿瘤药物的递送,突破纳米药物在实体瘤中的渗透性瓶颈。目前该产品已先后于2023年12月、2024年7月在美国和中国获批临床,拟用于单独治疗晚期/转移性实体瘤。
注射用PL002为荧光/磁共振双模态造影剂,计划用于肝癌的术中荧光导航及术前辅助诊断。据悉,本品采用独特的钆络合物与荧光分子共价键结合的分子结构设计,通过核磁共振成像(MRI)对荧光分子在肿瘤部位的富集情况进行确定,能提前判断病灶及正常组织的荧光标记情况,进而帮助医生为患者提供更精准的术前规划,降低手术难度和风险。目前,该产品已于2023年10月在美国获批临床,2024年9月在中国申报临床获受理。
本文来源:财经报道网










